
【题目】下列说法正确的是( )
A. 可用丁达尔现象区分溶液与胶体
B. 生石灰与水混合的过程只发生物理变化
C. O3是由3个氧原子构成的化合物
D. CuSO4·5H2O是一种混合物
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某校研究性学习小组的同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列研究:
【制取氨气】
(1)实验室常用加热氯化铵和氢氧化钙固体混合物的方法来制取氨气,该方法制备氨气的装置为_____(填字母,下同),收集氨气的装置可以是__________。
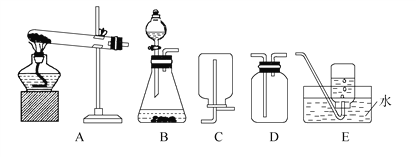
【实验探究】
该小组设计实验探究氨气的还原性及其产物,实验装置图(夹持装置未画出)如下:
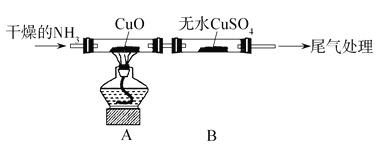
(2)通入的NH3必须干燥的原因是__________________。
(3)实验中观察到CuO变为红色物质,无水CuSO4变蓝,同时生成一种无污染的气体。请写出NH3与CuO反应的化学方程式:_____________________。
【问题讨论】
有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O.已知Cu2O是红色粉末,是一种碱性氧化物,在酸性溶液中,Cu+能自身发生氧化还原反应生成Cu2+和Cu.请你设计一个简单的实验检验该红色物质中是否含有Cu2O:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的,你认为其中的原因可能是( )
A. 向容量瓶中加水未到刻度线
B. 所用NaOH已经潮解
C. 定容时未洗涤烧杯和玻璃棒
D. 用带游码的托盘天平称2.4gNaOH 时误用了“左码右物”方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是 ( )
A .分液、萃取、蒸馏 B .分液、蒸馏、萃取
C. 萃取、蒸馏、分液 D. 蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.同温同压下,H2(g)+Cl2(g)= 2HCl(g)在光照和点燃条件下的△H相同
C.生成物的总焓大于反应物的总焓时,反应放热,ΔH<0
D.ΔH的大小与热化学方程式的化学计量数无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
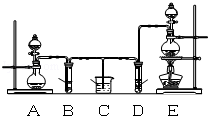
(1)他们制备Cl2依据的原理是:MnO2+4HCl(浓)△MnCl2+2H2O+Cl2↑,应选用图A、E装置中的 (填序号)制Cl2,反应中浓盐酸所表现出的性质是 、 .
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是 .
(3)写出过量NaOH溶液与SO2气体反应的离子方程式是 .
(4)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色.查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,充分燃烧一定量的丁烷放出热量为Q kJ(Q>0),经测定完全吸收生成的CO2需消耗 5 mol·L-1的KOH溶液100 mL,恰好生成正盐,则此条件下反应C4H10(g)+O2(g)===4CO2(g)+5H2O(g)的ΔH为
A.+8Q kJ·mol-1 B. -16Q kJ·mol-1
C.-8Q kJ·mol-1 D. +16Q kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出表示含有8个质子,10个中子的原子的化学符号:____________。
(2)已知阴离子aX2-和阳离子bYn+具有相同的核外电子排布,则a、b、n之间的关系为a=________。
(3)某元素的一种核素的质量数为A,含N个中子,它与1H原子组成HmX分子,在a g HmX中所含质子的物质的量为________mol。
(4)某元素R气态氢化物的化学式为RH3,其最高价氧化物中含氧量为![]() ,已知该元素的原子核内质子数和中子数相等,则该元素的名称为________。
,已知该元素的原子核内质子数和中子数相等,则该元素的名称为________。
(5)下列物质中:①氩单质 ②MgCl2 ③NH4Cl ④CH4 ⑤CO2 ⑥金刚石 ⑦H2SO4 ⑧KOH ⑨Na2O2 ⑩K2O
只存在共价键的是_______(填序号);
属于离子化合物,但含有极性共价键的是______(填序号)。
(6)如图所示每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是______
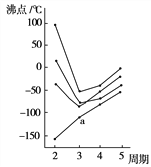
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种元素的原子序数大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同且电子总数为30;D和E可形成4核10电子分子。回答:
(1)写出五种元素的名称:A____B____C____D___E_____
(2)用电子式表示离子化合物A2B的形成过程:___________________________
(3)写出D元素形成的单质的结构式____________
(4)A、B两元素组成的化合物A2B2中存在的化学键是____________,写出A2B2与CO2反应的化学反应方程式________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com