
下图所示实验装置用于测定气体摩尔体积,相关叙述正确的是 ( )。
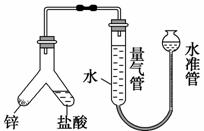
A.用CCl4代替水,测得氢气的体积更准确
B.量气管压入漏斗的水过多而溢出,会导致测定失败
C.必须待体系温度降低到0 ℃时才可进行读数
D.上提水准管,量气管液面高度不断改变,说明装置漏气
 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
(1)盖斯是热化学的奠基人,于1840年提出盖斯定律,利用这一定律可以从已经精确测定的反应热效应来计算难于测量或不能测量的反应的热效应.
已知:N2(g)+2O2(g)═2NO2(g)△H=+67.7kJ•mol﹣1,
N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=﹣534kJ•mol﹣1.
请写出气态肼与NO2气体完全反应生成氮气和水蒸气的热化学方程式: .
(2)已知:N≡N的键能是946kJ•mol﹣1,H﹣H的键能为436kJ•mol﹣1,N﹣H的键能为393kJ•mol﹣1,计算合成氨反应生成1molNH3的△H= kJ•mol﹣1.
(3)现有25℃、pH=13的Ba(OH)2溶液,
①该Ba(OH)2溶液的物质的量浓度为
②加水稀释100倍,所得溶液中由水电离出c(OH﹣)=
③与某浓度盐酸溶液按体积比(碱与酸之比)1:9混合后,所得溶液pH=11,该盐酸溶液的pH= .
(4)回答醋酸与氢氧化钠反应的有关问题
①将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 (填“酸性”,“中性”或“碱性”,下同),溶液中c(Na+) c(CH3COO﹣)(填“>”或“=”或“<”).
②pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 ,溶液中c(Na+) c(CH3COO﹣).
③物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 ,醋酸体积 氢氧化钠溶液体积.
查看答案和解析>>
科目:高中化学 来源: 题型:
A~G是几种烃的分子球棍模型(如图)

据此回答下列问题:
(1)常温下含碳量最高的气态烃是 (填对应字母).
(2)能够发生加成反应的烃有(填数字) 种.
(3)一卤代物种类最多的是(填对应字母) .
(4)写出实验室制取C的化学方程式 .
(5)写出F发生溴代反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有________(填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系。
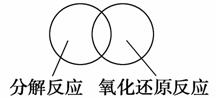
(3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。
| ①所有的离子方程式均可以表示一类反应 | |
| ②酸碱中和反应均可表示为H++OH-===H2O | |
| ③离子方程式中凡是难溶性酸、碱、盐均要标“↓”符号 |
(4)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“Ba2++SO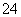 ===BaSO4↓”来表示,请写出有关反应的化学方程式(3个):
===BaSO4↓”来表示,请写出有关反应的化学方程式(3个):
①_______________________________________________________________;
②_______________________________________________________________;
③_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关合金的性质叙述不正确的是 ( )。
A.合金的熔点比它的各成分金属的熔点低
B.合金一定是金属熔合而成的
C.合金的硬度和强度一般比纯金属高
D.硬铝、黄铜、钢均为合金
查看答案和解析>>
科目:高中化学 来源: 题型:
目前市场上有大量的铝质罐装饮料,采用铝质易拉罐的原因可能考虑的因素有 ( )。
①铝矿储量较丰富,原料成本低 ②包装、运输、存放等方面比较方便、易
行 ③用过的铝质易拉罐可以回收再利用 ④铝制品对人体健康没有不良影
响,可以放心使用
A.①②③ B.②③④ C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列广告语中,你认为符合科学道理的是 ( )。
A.“超纯水”“超纯蒸馏水”绝对卫生,对人体有益
B.本饮料由纯天然物质配制而成,绝对不含化学物质,对人体无害
C.含氟牙膏可以预防龋齿
D.含碘食盐可防止贫血
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D是原子序数依次增大的四种短周期元素,它们分别按原子个数1∶1组成甲、乙、丙、丁四种物质。已知:甲由A、B组成,常温为气态;乙由A、C组成,常温为液态;丙由A、D组成,丁由C、D组成,丙、丁均为离子化合物。
根据以上信息回答:
(1)D在周期表中处于第________周期________族;乙的电子式为________;丙的化学式为________。
(2)丁遇水易变质,请用化学方程式解释:______________________。
(3)标准状况下,5.6 L甲完全燃烧生成稳定氧化物放出325 kJ热量,则甲燃烧热的热化学方程式为___________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com