
��ҵ�������̿�MnCO3���ۺ�FeCO3��SiO2��Cu2��OH��2CO3�����ʣ�Ϊԭ����ȡ�������̣�������ʾ��ͼ���£�
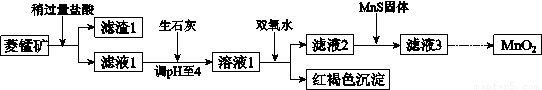
��֪�������������������pH
Mn��OH��2 | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | |
��ʼ����ʱ | 8.3 | 6.3 | 2.7 | 4.7 |
��ȫ����ʱ | 9.8 | 8.3 | 3.7 | 6.7 |
ע���������ӵ���ʼŨ��Ϊ0.1 mol/L
�ش��������⣺
��1�������ʵ����̿�ʹ��ǰ�轫����飬��ҪĿ���� ��
�����ܽ�MnCO3�Ļ�ѧ����ʽ�� ��
��2������Һ1�м���˫��ˮʱ����Ӧ�����ӷ���ʽ�� ��
��3����MnCl2ת��ΪMnO2��һ�ַ���������������������������ữ��NaClO3��Һ��MnCl2�������÷�Ӧ�����ӷ���ʽΪ����Mn2������ClO3������H2O����Cl2����________����________��
��4����MnCl2ת��ΪMnO2����һ�ַ����ǵ�ⷨ��
�� ����MnO2�ĵ缫��Ӧʽ�� ��
�� ��ֱ�ӵ��MnCl2��Һ������MnO2��ͬʱ���������Cl2������Cl2�IJ����� ��
�� ��������MnCl2��Һ�м���һ������Mn��NO3��2��ĩ������Cl2��������ԭ���� ��
 ���ſ����ϵ�д�
���ſ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ܱ������н������·�Ӧ��X2��g��+Y2��g��  2Z��g������֪X2��Y2��Z����ʼŨ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.2mol/L����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п�����
2Z��g������֪X2��Y2��Z����ʼŨ�ȷֱ�Ϊ0.1mol/L��0.3mol/L��0.2mol/L����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п�����
A�� ZΪ0.3mol/L B�� Y2Ϊ0.4mol/L
C�� X2Ϊ0.2mol/L D�� ZΪ0.4mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
��8�֣���Cl2����ijЩ�����л���ʱ�����������HCl�����÷�ӦA����ʵ���ȵ�ѭ�����á�
��ӦA��

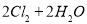
��֪��i����ӦA�У�2mol ���ӷ���ת�ƣ��ų�57��8kJ��������
ii��
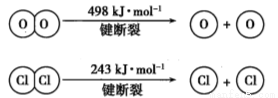
��H2O�ĵ���ʽ�� ��
�ڷ�ӦA���Ȼ�ѧ����ʽ�� ��
�۶Ͽ�1mol H-O����Ͽ�1mol H-Cl������������� kJ��H2O��H-O����HCl��H-Cl�� ���ǿ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ�����и�����ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����������͢����ȷ�����������ϵ����
ѡ�� | ������ | ������ |
A | Na2S��ǿ��ԭ�� | ���ڳ�ȥ��ˮ�е�Cu2+��Hg2+ |
B | CaCO3�������� | CaCl2��Һ��ͨ��CO2������ɫ���� |
C | ŨH2SO4��ǿ������ | ŨH2SO4�����ڸ���SO2 |
D | Zn���л�ԭ�Ժ͵����� | ������п�̸ɵ�صĸ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ���Ʊ��Ȼ�ͭʱ���ǽ�Ũ����������������80 �����ң����������������ͭ��ĩ����������������������ֽ��裬ʹ֮�ܽ⣬��Ӧ����: CuO+2HCl=CuCl2+H2O��FeO+2HCl=FeCl2+H2O����֪: ��pH��9.6ʱ��Fe2+��Fe��OH��2��ʽ��ȫ����; pH��6.4ʱ�� Cu2+��Cu��OH��2��ʽ��ȫ����;pH��3��4ʱ�� Fe3+��Fe��OH��3��ʽ��ȫ��������ȥ��Һ�е�Fe2+���Բ��õķ�����
A��ֱ�ӼӼ������ҺpH��9.6
B���Ӵ�ͭ�ۣ���Fe2+��ԭ����
C���Ƚ�Fe2+����Fe3+���ٵ���pH��3��4
D��ͨ�����⣬ʹFe2+ֱ�ӳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ�����и�����ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��4 mol A�����2 mol B������2 L�������л�ϲ���һ�������·������·�Ӧ��2A��g��+B��g�� 2C��g��������2 s����C��Ũ��Ϊ0.6 mol��L-1���������м���˵������������A��ʾ�ķ�Ӧƽ������Ϊ0.3 mol��L-1��s-1����������B��ʾ�ķ�Ӧ��ƽ������Ϊ0. 6 mol��L-1��s-1����2 sʱ����A��ת����Ϊ70%����2 sʱ����B��Ũ��Ϊ0.7 mol��L-1��������ȷ����
2C��g��������2 s����C��Ũ��Ϊ0.6 mol��L-1���������м���˵������������A��ʾ�ķ�Ӧƽ������Ϊ0.3 mol��L-1��s-1����������B��ʾ�ķ�Ӧ��ƽ������Ϊ0. 6 mol��L-1��s-1����2 sʱ����A��ת����Ϊ70%����2 sʱ����B��Ũ��Ϊ0.7 mol��L-1��������ȷ����
A���٢� B���٢� C���ڢ� D���ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡУ������ѧ�ڽ��Կ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶��£���C12ͨ��NaOH��Һ�У���Ӧ�õ�NaCl��NaClO��NaClO3�Ļ��Һ�����ⶨNaClO��NaClO3��Ũ��֮��Ϊ1:3����Cl2��NaOH��Һ��Ӧʱ����ԭ����Ԫ���뱻��������Ԫ�ص����ʵ���֮��Ϊ
A��21:5 B�� 11:3 C��3:1 D��4:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ�ĵ���У������ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ײ�����ȱλ�����Σ�MFe2Ox ����3��x��4��M��ʾMn��Co��Zn��Ni�Ķ������ӣ��������£�����ʹ��ҵ�����е�SO2��NO2��������ת��Ϊ���ʣ�ת��������ͼ��ʾ���й�����ת�����̵�����������ȷ����
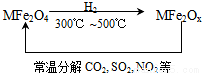
A��MFe2O4�����˻�ԭ�� B��MFe2Ox�����˻�ԭ��
C��SO2��NO2�����˻�ԭ�� D��SO2��NO2�����˷ֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ڱ�״���£��ݻ�Ϊ1 L���ܱ������иպÿ���ʢ��a��N2���Ӻ�b��H2������ɵĻ�����壬���ӵ������Ľ���ֵ���Ա�ʾΪ
A��a+b B��22.4 (a+b) ��6.02��1023
C��22.4 (a+b) / 6.02��1023 D��22.4 (a+b)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com