
| A.工业生产中常用生石灰来吸收废气中的二氧化硫 |
| B.二氧化硫的水溶液能使紫色石蕊试液变红,说明二氧化硫能与水反应生成酸 |
| C.二氧化硫能使有色物质颜色消失,说明二氧化硫具有氧化性 |
| D.二氧化硫能使酸性高锰酸钾溶液褪色,说明二氧化硫具有还原性 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.将SO2气体通入到溴水中使溴水褪色 |
| B.将SO2气体通入到KMnO4溶液中使KMnO4,溶液褪色 |
| C.将SO2气体通入到滴有酚酞的NaOH溶液中,溶液褪色 |
| D.将SO2气体通入到氯水中使氯水褪色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硫单质与金属铁反应生成FeS,体现了硫单质的氧化性 |
| B.H2S既具有还原性,又具有氧化性 |
| C.SO2能使酸性KMnO4溶液、氯水褪色,说明SO2具有漂白性。 |
| D.SO2在一定条件下可转化为SO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
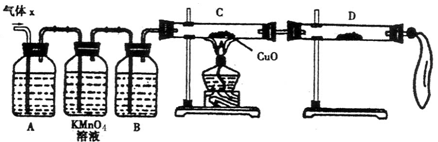
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
|
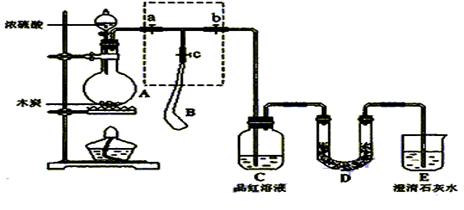 请回答下列问题:
请回答下列问题:  分的装置,则正确的操作
分的装置,则正确的操作 顺序是 (用操作编号填写)
顺序是 (用操作编号填写) 水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该实验表明SO2有漂白性 | B.白色沉淀为BaSO4 |
| C.该实验表明FeCl3有氧化性 | D.反应后溶液酸性增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com