
| A. | CO2和H2O | B. | NaCl和HCl | C. | SO2和SiO2 | D. | NaOH和CCl4 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键;由分子构成的晶体为分子晶体,由离子构成的晶体为离子晶体,由原子构成且存在共价键的为原子晶体,以此来解答.
解答 解:A.均只含共价键,均由分子构成,则均属于分子晶体,故A选;
B.NaCl中含离子键,为离子晶体;而HCl中含共价键,由分子构成为分子晶体,故B不选;
C.均含共价键,SO2由分子构成为分子晶体,而SiO2由原子构成为原子晶体,故C不选;
D.NaOH中含离子键和共价键,为离子晶体;CCl4中含共价键,由分子构成为分子晶体,故D不选;
故选A.
点评 本题考查化学键及晶体类型,为高频考点,把握化学键的形成及判断的一般规律、晶体的构成微粒及作用力为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A. | 相对分子质量相同,结构不同的有机物互为同分异构体 | |
| B. | 同分异构体间的相互转化一定伴随着能量的变化 | |
| C. | C4H10的一氯取代物共有4种结构 | |
| D. | 甲苯( )苯环上的氢原子被一个氯原子取代,共有3种同分异构体 )苯环上的氢原子被一个氯原子取代,共有3种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 甲醛在酸性催化剂存在下三分子聚合可以生成性质相对稳定、毒性小、易于运输的三聚甲醛,反应如图所示.下列说法正确的是( )
甲醛在酸性催化剂存在下三分子聚合可以生成性质相对稳定、毒性小、易于运输的三聚甲醛,反应如图所示.下列说法正确的是( )| A. | 甲醛水溶液可作为食物防腐剂 | |
| B. | 该反应类型为缩聚反应 | |
| C. | 三聚甲醛分子中既含σ键又含п键 | |
| D. | 常温下,9g三聚甲醛中含1.806×1023个碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;NH3在同族元素形成的氢化物中具有较高的沸点,其原因是NH3分子间有氢键.
;NH3在同族元素形成的氢化物中具有较高的沸点,其原因是NH3分子间有氢键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3-CH2-CH2Br | B. | CH3-CHBr-CH2Br | C. | CH3-CH2-CHBr | D. | CH3-CHBr-CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
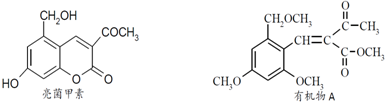


 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
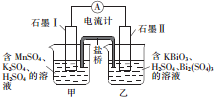 已知KBiO2+MnSO4+H2SO4→Bi2(SO4)3+KMnO4+H2O+K2SO4(未配平),利用上述化学反应设计成如图所示原电池(盐桥中装有含琼胶的饱和K2SO4溶液),下列说法正确的是( )
已知KBiO2+MnSO4+H2SO4→Bi2(SO4)3+KMnO4+H2O+K2SO4(未配平),利用上述化学反应设计成如图所示原电池(盐桥中装有含琼胶的饱和K2SO4溶液),下列说法正确的是( )| A. | 电池工作时,电子移向为石墨Ⅰ→溶液→盐桥→溶液→石墨Ⅱ | |
| B. | 电池工作时,盐桥中的K+移向甲烧杯 | |
| C. | 甲烧杯中发生的电极反应为Mn2+-4e-+4H2O═MnO4-+8H+ | |
| D. | 电池工作一段时间后乙烧杯中溶液的pH增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com