
| A、正戊烷和正己烷 |
| B、苯和丙烷 |
| C、对二甲苯和2,2-二甲基丙烷 |
| D、甲苯和2-甲基丙烷 |


科目:高中化学 来源: 题型:
| A、25°C时,pH=3的1.0L NaHSO3溶液中,含Na+数目为0.001 NA |
| B、0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3NA |
| C、2.3g甲苯和丙三醇的混合物中,含氢原子数目为0.2 NA |
| D、标准状况下,22.4L乙醇中含有的氧原子数为1.0NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钙和醋酸 CaCO3+2H+═Ca2++H2O+CO2↑ | ||||
| B、碳酸氢钙溶液和足量氢氧化钠溶液 Ca2++HCO3-+OH-=CaCO3↓+H2O | ||||
| C、铜和稀硝酸反应 Cu+4H++NO3?═Cu2++NO↑+2H2O | ||||
D、硫酸铵溶液和氢氧化钠溶液共热 NH4++OH-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烷和氯气光照下制取纯净的氯乙烷 |
| B、用分液漏斗分离环己烷和水的混合液体 |
| C、用浓氨水洗涤做过银镜反应的试管 |
| D、在苯和溴水的混合物中加入铁粉制取溴苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、鉴别集气瓶中的甲烷和乙烯:移去玻璃片,分别点燃,观察火焰的颜色及是否有黑烟 |
| B、检验酒精中的少量水:向酒精中加入足量生石灰 |
| C、制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应 |
| D、除去乙炔中杂质气体:将实验室制得的乙炔气体通入硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、比较多电子原子中电子能量大小的依据是电子离原子核的远近 |
| B、各能级最多容纳的电子数是该能级原子轨道数的二倍,其理论依据是构造原理 |
| C、电子排布在同一能级时,总是自由配对,优先占据同一轨道,且自旋方向相反 |
| D、钠的焰色与原子核外电子发生跃迁有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L SO3所含分子数为0.5 NA |
| B、1L 1mol/L的氯化钠溶液中,所含离子数为NA |
| C、64g二氧化硫含有原子数为3NA |
| D、在反应中,1mol镁转化为Mg2+后失去的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
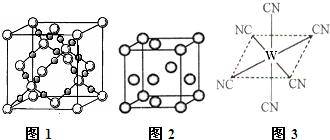
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作步骤 | |
| 反应现象 | |
| 结论 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com