
| A. | 0.002 0 | B. | 0.011 | C. | 0.11 | D. | 0.22 |
分析 根据反应前后溶液中氢离子的物质的量不变计算出加入的pH=1的盐酸的体积,根据总体积计算出加入的硝酸银溶液的体积;根据关系式Ag+~Cl-计算出硝酸银的物质的量,再根据c=$\frac{n}{V}$计算出硝酸银溶液的浓度.
解答 解:pH=2的溶液中氢离子浓度为0.01mol/L,100mL该溶液中含有氢离子的物质的量为:0.01mol/L×0.1L=0.001mol,说明加入盐酸中含有氯化氢的物质的量为0.001mol;
pH=1的盐酸的浓度为0.1mol/L,则加入pH=1的盐酸的体积为:$\frac{0.001mol}{0.1mol/L}$=0.01L=10mL,
反应前后溶液体积变化忽略不计,则加入硝酸银溶液的体积为:100mL-10mL=90mL,
根据关系式Ag+~Cl-可知,硝酸银的物质的量为0.001mol,则加入的硝酸银的浓度为:$\frac{0.001mol}{0.09L}$≈0.011mol/L,
故选B.
点评 本题考查了物质的量浓度的计算、溶液pH计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握物质的量浓度的概念及计算方法,试题培养了学生的分析能力及化学计算能力.


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案科目:高中化学 来源: 题型:填空题
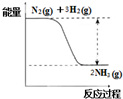 在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系.
在已经发现的一百多种元素中,除稀有气体外,非金属元素只有十多种,但与生产生活有密切的联系.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙炔和苯均为不饱和烃,都能发生加成反应 | |
| B. | 加新制的Cu(OH)2悬浊液并加热可检验尿液中的葡萄糖 | |
| C. | 油脂在酸的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 水果因含有酯类物质而具有香味 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含有一种元素的物质一定是纯净物 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | 石墨转变为金刚石为化学变化 | |
| D. | 水很稳定是因为水分子间存在较强的分子间作用力 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| B. | 某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 | |
| C. | 某无色溶液中加Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,则原溶液中一定有SO42- | |
| D. | 在蔗糖与稀硫酸共热后的溶液中加入新制Cu(OH)2,加热煮沸,会生成砖红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
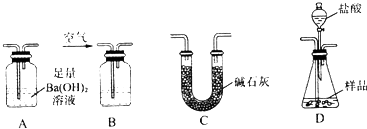
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe+2H+═Fe2++H2↑ | B. | 2Fe3++Cu═2Fe2++Cu2+ | ||
| C. | 2H2+O2═2H2O | D. | H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
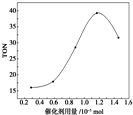 在催化剂作用下,可由甲醇和CO2直接合成碳酸二甲酯:CO2+2CH3OH-→CO(OCH3)2+H2O.某研究小组在其他条件不变的情况下,通过研究催化剂用量分别对转化数(TON)的影响来评价催化剂的催化效果.计算公式为TON=转化的甲醇的物质的量/催化剂的物质的量.根据该研究小组的实验及催化剂用量TON的影响图,判断下列说法不正确的是( )
在催化剂作用下,可由甲醇和CO2直接合成碳酸二甲酯:CO2+2CH3OH-→CO(OCH3)2+H2O.某研究小组在其他条件不变的情况下,通过研究催化剂用量分别对转化数(TON)的影响来评价催化剂的催化效果.计算公式为TON=转化的甲醇的物质的量/催化剂的物质的量.根据该研究小组的实验及催化剂用量TON的影响图,判断下列说法不正确的是( )| A. | 由甲醇和CO2直接合成碳酸二甲酯,可以利用价廉易得的甲醇把影响环境的温室气体CO2转化为资源,在资源循环利用和环境保护方面都具有重要意义 | |
| B. | 在反应体系中添加合适的吸水剂,将提高该反应的TON | |
| C. | 当催化剂用量为1.2×10-5 mol时,该反应的TON达到最高点 | |
| D. | 当催化剂用量高于1.2×10-5 mol时,随着催化剂用量的增加,甲醇的平衡转化率逐渐降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,电池总反应为:4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )
我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,电池总反应为:4Al+3O2+6H2O═4Al(OH)3.下列关于该电池的说法不正确的是( )| A. | 铝板是电池的正极 | |
| B. | 电池工作时铝板逐渐被消耗 | |
| C. | 电池工作时实现了化学能向电能的转化 | |
| D. | 将铂电极做成网状,可增大与氧气的接触面积 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com