
| A、3种 | B、4种 | C、5种 | D、6种 |


 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:
| 元素 | 相关信息 |
| X | X的基态原子价电子排布式为:nsnnpn+1 |
| Y | Y原子的最外层电子数是次外层的三倍 |
| Z | Z存在质量数为27,中子数为14的核素 |
| W | W元素最高价氧化物对应的水化物是一种不溶于水的蓝色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子总数 | B、密度 |
| C、质量 | D、质子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ |
| B、Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ |
| C、将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
| D、用酸性KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++7H2O2═2Mn2++6O2↑+10H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
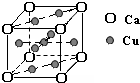 【物质结构域性质】
【物质结构域性质】查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
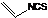 是一种天然植物杀虫剂,其中N原子的杂化方式为sp3
是一种天然植物杀虫剂,其中N原子的杂化方式为sp3查看答案和解析>>
科目:高中化学 来源: 题型:
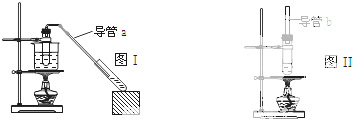
| A、制乙酸乙酯用图I装置,制乙酸丁酯用图II 装置 |
| B、导管a和导管b的作用都是冷凝回流 |
| C、都可用Na2CO3 溶液来洗去酯中的酸和醇 |
| D、加入过量的乙酸可以提高醇的转化率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com