
| A、5.0L | B、8.9L |
| C、15.7L | D、26.9L |
| 12g |
| 80g/mol |
| 12g |
| 80g/mol |
| V |
| 22.4L/mol |
| V |
| 22.4L/mol |


科目:高中化学 来源: 题型:

| A、S-诱抗素制剂能发生酯化反应的官能团有2种 |
| B、含有苯环、羟基、羰基、羧基、碳碳双键 |
| C、1mol S-诱抗素制剂与足量金属Na反应生成0.5mol H2 |
| D、该化合物不能发生聚合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图表示ⅡA金属(又称为碱金属)的某些性质与核电荷数的变化关系,则下列各性质中不符合图示关系的是( )
如图表示ⅡA金属(又称为碱金属)的某些性质与核电荷数的变化关系,则下列各性质中不符合图示关系的是( )| A、金属性 |
| B、与水反应的剧烈程度 |
| C、阳离子的氧化性 |
| D、原子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(F-)=2×10-4 mol?L-1 |
| B、c(F-)=5×10-5 mol?L-1 |
| C、c(Sr2+)=4.5×10-2 mol?L-1 |
| D、c(Sr2+)=0.1 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水的屯离程度:①<② |
| B、①、②中粒子浓度关系均符合:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(co32-) |
| C、向③、④中分别加入25 mL 0.l mol?L-1盐酸后,溶液中c(NH4+):③<④ |
| D、将③、④混合,所得溶液的pH>7,则该溶液中:c(NH4+)=c(NH3?H2O) |
查看答案和解析>>
科目:高中化学 来源: 题型:
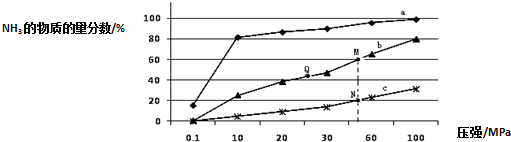

查看答案和解析>>
科目:高中化学 来源: 题型:
 某温度时,在容积为2L的密闭容器中,x、y、z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答:
某温度时,在容积为2L的密闭容器中,x、y、z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
 目前混合动力车使用的镍氢电池如图所示,在碱性环境下,镍氢电池充放电总反应式为:H2+NiOOH
目前混合动力车使用的镍氢电池如图所示,在碱性环境下,镍氢电池充放电总反应式为:H2+NiOOH| 充电 |
| 放电 |
| A、放电时,甲电极的电极反应式为:H2 +2e-═2H+ |
| B、放电时,OH-通过交换膜向甲极移动 |
| C、充电时,甲电极附近的pH变小 |
| D、充电时,乙电极质量增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com