
| A、金属性逐渐增强 |
| B、原子半径逐渐增大 |
| C、最高正价数值逐渐减小 |
| D、从硅到氯负价从-4→-1 |


科目:高中化学 来源: 题型:
| A、开始滴加氨水时形成的难溶物为Cu(OH)2 |
| B、沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4]2+,配位数为2 |
| C、反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
| D、在[Cu(NH3)4]2+中,Cu2+给出孤电子对,NH3提供空轨道 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向NaAlO2溶液中通入过量CO2制Al(OH)3:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| B、向Fe(NO3)3溶液中加入过量的HI溶液:2NO3-+8H++6I-=3I2+2NO↑+4H2O |
| C、用硫酸酸化的淀粉碘化钾溶液在空气中变蓝:4I-+O2+4H+=2I2+2H2O |
| D、向NH4Al(SO4)2溶液中滴加Ba(OH)2恰好使SO42-反应完全:2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
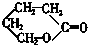 ⑥
⑥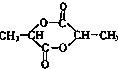 ⑦
⑦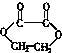 ⑧
⑧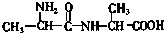
| A、①②③ | B、④⑤⑧ |
| C、②⑥⑧ | D、①⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铬位于元素周期表的第四周期第Ⅷ族 | ||
B、中子数为29的铬原子符号表示为
| ||
| C、已知铬元素的一种同位素的质量数为53,则该同位素有53个中子 | ||
| D、警察通过装有橙色的酸性重铬酸钾的装置检查司机是否酒后驾车 |
查看答案和解析>>
科目:高中化学 来源: 题型:

 中的配位键.
中的配位键.
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com