
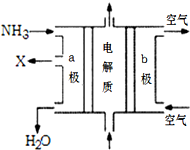
 以下是对化学反应变化过程及结果的研究.按要求回答问题:
以下是对化学反应变化过程及结果的研究.按要求回答问题:| c(CH 3COO -)?c(H +) |
| c(CH 3COOH) |
| c(CH 3COO -)?c(H +) |
| c(CH 3COOH) |
| 10 -b×10 -b |
| 10 a-14-10 -b |
| 10 -2b |
| 10 a-14-10 -b |
| 10 -2b |
| 10 a-14-10 -b |
| 4.48L |
| 22.4L/mol |


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
| A、该合金的熔点高于金属钠的熔点 |
| B、若将钠铝合金投入水中得到无色溶液且无固体剩余,则n(Al)>n(Na) |
| C、若将钠铝合金投入FeCl3溶液中有Fe(OH)3沉淀生成 |
| D、等质量的钠铝合金中铝的含量越大,与足量盐酸反应时放出的氢气越少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
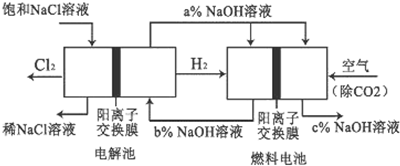
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、合成氨工业中,移走NH3可增大正反应速率,提高原料转化率 |
| B、酸碱中和滴定时,锥形瓶需用待测液润洗2次,再加入待测液 |
| C、将NO2、N2O4混合气体的体积压缩为原来的一半,则气体颜色加深 |
| D、牺牲阳极的阴极保护法和外加直流电源的阴极保护法都是应用电解原理 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、缩小体积使压强增大 |
| B、降低体系温度 |
| C、体积不变充入He使气体压强增大 |
| D、保持总压强不变,充入Ne气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
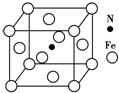 铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂.
铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(-NO2)还原为氨基(-NH2);在苯的溴代反应中用溴化铁作催化剂.查看答案和解析>>
科目:高中化学 来源: 题型:
 “暖冰”是韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成的.某老师在课堂上做了一个如右图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN 的FeCl2溶液,则溶液呈血红色.则下列说法中不正确的是( )
“暖冰”是韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成的.某老师在课堂上做了一个如右图所示的实验,发现烧杯中酸性KMnO4溶液褪色.若将烧杯中的溶液换成含有少量KSCN 的FeCl2溶液,则溶液呈血红色.则下列说法中不正确的是( )| A、在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
| B、该条件下H2燃烧的产物中可能含有一定量的H2O2 |
| C、该条件下H2燃烧生成了既具有氧化性又具有还原性的物质 |
| D、水凝固形成20℃时的“暖冰”所发生的变化是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1-丁烯 |
| B、甲苯 |
| C、二甲苯 |
| D、2-甲基-3-乙基-2-戊烯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com