
 某气态烃A在标准状况下的密度是1.875g/L.其核磁共振氢谱有三组峰,峰面积比为2:1:3.A有如图转化关系:
某气态烃A在标准状况下的密度是1.875g/L.其核磁共振氢谱有三组峰,峰面积比为2:1:3.A有如图转化关系:



分析 气态烃A在标准状况下的密度是1.875g/L,则A的相对分子质量为1.875×22.4=42,其核磁共振氢谱有三组峰,峰面积比为2:1:3,则A为CH3CH=CH2,根据各物质转化关系,A与苯发生信息中的加成反应生成B,C是B的一溴代物,B发生取代反应生成C,C碱性水解得F,F不能在Cu做催化剂的条件下被O2氧化,则可推知B为 ,C为
,C为 ,F为
,F为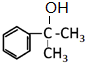 ,F在浓硫酸的作用下也能生成D,E是一种高聚物,D发生加聚反应生成E,则D为
,F在浓硫酸的作用下也能生成D,E是一种高聚物,D发生加聚反应生成E,则D为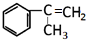 ,E为
,E为 ,根据G的分子式可知,C与钠反应生成G为
,根据G的分子式可知,C与钠反应生成G为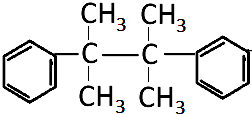 ,H的相对分子质量是165,其苯环上的一氯代物有两种,B发生硝化反应生成H为
,H的相对分子质量是165,其苯环上的一氯代物有两种,B发生硝化反应生成H为 ,据此答题.
,据此答题.
解答 解:气态烃A在标准状况下的密度是1.875g/L,则A的相对分子质量为1.875×22.4=42,其核磁共振氢谱有三组峰,峰面积比为2:1:3,则A为CH3CH=CH2,根据各物质转化关系,A与苯发生信息中的加成反应生成B,C是B的一溴代物,B发生取代反应生成C,C碱性水解得F,F不能在Cu做催化剂的条件下被O2氧化,则可推知B为 ,C为
,C为 ,F为
,F为 ,F在浓硫酸的作用下也能生成D,E是一种高聚物,D发生加聚反应生成E,则D为
,F在浓硫酸的作用下也能生成D,E是一种高聚物,D发生加聚反应生成E,则D为 ,E为
,E为 ,根据G的分子式可知,C与钠反应生成G为
,根据G的分子式可知,C与钠反应生成G为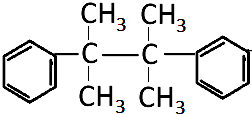 ,H的相对分子质量是165,其苯环上的一氯代物有两种,B发生硝化反应生成H为
,H的相对分子质量是165,其苯环上的一氯代物有两种,B发生硝化反应生成H为 ,
,
(1)根据上面的分析可知,A为CH3CH=CH2,故答案为:CH3CH=CH2;
(2)根据上面的分析可知,B转化为C的反应类型是取代反应,故答案为:取代反应;
(3)根据上面的分析可知,C为 ,故答案为:
,故答案为: ;
;
(4)①D为 ,D能发生的反应有氧化反应、取代反应、加成反应,故选bcd;
,D能发生的反应有氧化反应、取代反应、加成反应,故选bcd;
②E的结构简式是 ,故答案为:
,故答案为: ;
;
(5)B转化为H的化学方程式是  ,
,
故答案为: ;
;
(6)G为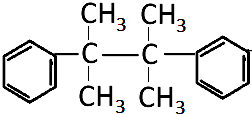 ,其一氯代物有4种,故答案为:4;
,其一氯代物有4种,故答案为:4;
(7)F为 ,根据条件i.属于酚类; ii.苯环上的一溴代物有两种,则苯环上有两个处于对位的基团或有四个基团,所以符合条件的F的同分异构体为苯的对位上连有-OH、-CH(CH3)2或-OH、-CH2CH2CH3,或苯环上连有四个基团,分别为-OH、-CH3、-CH3、-CH3,有4种结构,所以共有6种,
,根据条件i.属于酚类; ii.苯环上的一溴代物有两种,则苯环上有两个处于对位的基团或有四个基团,所以符合条件的F的同分异构体为苯的对位上连有-OH、-CH(CH3)2或-OH、-CH2CH2CH3,或苯环上连有四个基团,分别为-OH、-CH3、-CH3、-CH3,有4种结构,所以共有6种,
故答案为:6.
点评 本题考查有机物推断,涉及烯、醇、羧酸、酯的性质与转化等,难度中等,注意同分异构体的判断方法,注意基础知识的理解掌握.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1molM最多可和1molNa2CO3发生反应 | |
| B. | 1molM最多可和6molH2发生加成反应 | |
| C. | 1molM最多可和3molNaOH反应 | |
| D. | 1molM最多可和2molNa反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一种具有除草功效的有机物的结构简式如图所示.下列有关该化合物的说法正确的是( )
一种具有除草功效的有机物的结构简式如图所示.下列有关该化合物的说法正确的是( )| A. | 分子式为C19H16O7 | |
| B. | 能发生氧化、取代、消去、加成反应 | |
| C. | 1 mol该化合物与足量浓溴水反应,最多消耗3 mol Br2 | |
| D. | 1 mol该化合物最多消耗4 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱、液态氧、冰水混合物 | B. | 生石灰、白磷、小苏打 | ||
| C. | 干冰、铁、氨水 | D. | 空气、氮气、胆矾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13.6克 | B. | 8.4克 | C. | 3.4 克 | D. | 2.8克 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg+2HCl═MgCl2+H2↑ | B. | 2NO+O2═2NO2 | ||
| C. | CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | D. | CaCl2+Na2CO3═CaCO3↓+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | A1 | B1 | C1 | D1 |
| 电子数 | 10 | 10 | 10 | 18 |
| ② | A2 | B2 | C2 | D2 |
| 电子数 | 10 | 10 | 10 | 18 |
 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com