
(1)当分别通入CO和O2时:
①正极反应:__________________________________________________;
②负极反应:__________________________________________________;
③电池总反应:________________________________________________;
④电解质溶液pH的变化__________。(填“增大”“减小”或“不变”)。
(2)当分别通入CH4和O2时:
①正极反应:__________________________________________________;
②负极反应:__________________________________________________;
③电池总反应:________________________________________________;
④电解质溶液pH的变化:________________。(填“增大”“减小”或“不变”)
(3)当分别通入H2S和Cl2时:
①正极反应:__________________________________________________;
②负极反应:__________________________________________________;
③电池总反应:________________________________________________;
④电解质溶液pH的变化:______________________________________。
(填“增大”“减小”或“不变”)
解析:燃料电池中,负极通入的燃料被氧化,C、S都被氧化到+4价,而+4价的C和S是不能单独存在的,在其常见存在形式CO2(或![]() )、SO2(或
)、SO2(或![]() )中,产物究竟是什么,O原子由谁来提供?应结合负极环境寻找答案。由于负极溶液是酸性的,所以不会生成
)中,产物究竟是什么,O原子由谁来提供?应结合负极环境寻找答案。由于负极溶液是酸性的,所以不会生成![]() 、
、![]() ,而是生成CO2、SO2逸出。在负极氛围中含O原子的粒子只有H2O分子(OH-极少而忽略),所以
,而是生成CO2、SO2逸出。在负极氛围中含O原子的粒子只有H2O分子(OH-极少而忽略),所以![]() (或
(或![]() )中的O原子无疑是由H2O分子提供的,提供O原子后的H2O分子将游离出H+。同时,若燃料中含H元素,则在C、S被氧化为CO2、SO2后,也释放出H+。负极反应式可根据电荷守恒而配平。
)中的O原子无疑是由H2O分子提供的,提供O原子后的H2O分子将游离出H+。同时,若燃料中含H元素,则在C、S被氧化为CO2、SO2后,也释放出H+。负极反应式可根据电荷守恒而配平。
若正极通入的气体为O2,则O2得电子变为O2-,O2-被H+俘获变为H2O分子。若正极的气体为Cl2,则Cl2得电子变为Cl-。
判断电解质溶液pH的变化,写出电池总反应式便知。这里将正、负电极反应式叠加,可得电池总反应。
答案:(1)①O2+4e-+4H+![]() 2H2O ②2CO+2H2O
2H2O ②2CO+2H2O![]() 2CO2+4H++4e-
2CO2+4H++4e-
③2CO+O2![]() 2CO2↑ ④不变
2CO2↑ ④不变
(2)①2O2+8e-+8H+![]() 4H2O ②CH4+2H2O
4H2O ②CH4+2H2O![]() CO2↑+8H++8e-
CO2↑+8H++8e-
③CH4+2O2![]() CO2↑+2H2O ④变大
CO2↑+2H2O ④变大
(3)①3Cl2+6e-![]() 6Cl- ②H2S+2H2O
6Cl- ②H2S+2H2O![]() 6H++SO2↑+6e-
6H++SO2↑+6e-
③3Cl2+H2S+2H2O![]() 6Cl-+6H++SO2↑ ④变小
6Cl-+6H++SO2↑ ④变小


科目:高中化学 来源: 题型:阅读理解
| 选项 | 铝电极 | 电解质 | 负极反应 | 正极反应 |
| A | 负极 | NaOH | 2Al-6e-+8OH-=2AlO2-+4H2O | 6H2O+6e-=6OH-+3H2↑ |
| B | 负极 | 稀盐酸 | 2Al-6e-=2Al3+ | 6H++6e-=3H2↑ |
| C | 正极 | 浓硝酸 | Mg+2e-=Mg2+ | 2NO3-+4H+-4e-=2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 选项 | 铝电极 | 电解质 | 负极反应 | 正极反应 |
| A | 负极 | NaOH | 2Al-6e-+8OH-=2AlO2-+4H2O | 6H2O+6e-=6OH-+3H2↑ |
| B | 负极 | 稀盐酸 | 2Al-6e-=2Al3+ | 6H++6e-=3H2↑ |
| C | 正极 | 浓硝酸 | Mg+2e-=Mg2+ | 2NO3-+4H+-4e-=2NO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 Al(OH)3+3H+,Cu2++2H2O
Al(OH)3+3H+,Cu2++2H2O Cu(OH)2+2H+,2Al+6H+=2Al3++3H2↑
Cu(OH)2+2H+,2Al+6H+=2Al3++3H2↑ Al(OH)3+3H+,Cu2++2H2O
Al(OH)3+3H+,Cu2++2H2O Cu(OH)2+2H+,2Al+6H+=2Al3++3H2↑
Cu(OH)2+2H+,2Al+6H+=2Al3++3H2↑| 选项 | 铝电极 | 电解质 | 负极反应 | 正极反应 |
| A | 正极 | NaOH | Al-3e-=Al3+ | 2H2O+2e-=2OH-+H2↑ |
| B | 负极 | 稀盐酸 | 2Al-6e-=2Al3+ | 6H++6e-=3H2↑ |
| C | 正极 | 浓硝酸 | Cu-2e--=Cu2+ | 2NO3-+4H+-4e-=2NO2↑+2H2O |
| D | 负极 | 稀硝酸 | Cu-2e-=Cu2+ | 2NO3-+8H+=2NO↑+4H2O+6e- |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 Cu(OH)2+2H+
Cu(OH)2+2H+ Cu(OH)2+2H+
Cu(OH)2+2H+
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
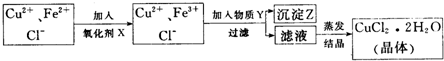
| 氢氧化物开始沉淀时的pH | 氯氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com