
如图都是简化的碳架结构:
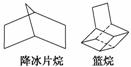
(1)其分子式分别是________、________。
(2)降冰片烷发生一氯取代时,取代位置有____________种。
(3)篮烷发生一氯取代时,其一氯代物有________种。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
将一定质量的Mg、Zn、Al的混合物与足量的稀H2SO4反应,生成H2 2.8 L(标准状况),原混合物的质量可能是( )
A.2 g B.4 g C.8 g D.10 g
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组对铝热反应实验展开研究。查阅有关资料后得知,“铝热反应”的现象为“反应放出大量的热,并发出耀眼的白光”、“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3的熔点和沸点数据如下:
| 物质 | Al | Al2O3 | Fe | Fe2O3 |
| 熔点/℃ | 660 | 2 054 | 1 535 | 1 462 |
| 沸点/℃ | 2 467 | 2 980 | 2 750 | — |
(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由:该反应放出的热量使铁熔化,而铝的熔点比铁的低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释________(填“合理”或“不合理”)。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是____________,反应的离子方程式为___________________。
(3)实验室溶解该熔融物,最适宜采用下列试剂中的________(填序号)。
A.浓硫酸 B.稀硫酸
C.稀硝酸 D.氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
能够证明甲烷构型是正四面体的事实是( )
A.甲烷的四个键键能相同
B.甲烷的四个键键长相等
C.甲烷的所有C—H键键角相等
D.二氯甲烷没有同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化工生产的说法中,不正确的是( )
A.工业上用热还原法冶炼铁:Fe2O3+3CO 3CO2+2Fe
3CO2+2Fe
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
C.在铁管上镀锌,用铁管作阳极,锌块作阴极
D.利用反应:NaCl(饱和)+CO2+NH3+H2O====NaHCO3↓+NH4Cl制取NaHCO3时,应先通入过量的NH3,再通入过量的CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
银铜合金广泛用于航空工业,从切割废料中回收银并制备铜化工产品的工艺如下:
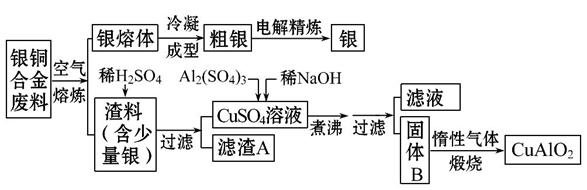
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为__________;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学反应方程式为____________
____________________________________________________。
(2)固体混合物B的组成为____________;在生成固体B的过程中,需控制NaOH的加入量。若NaOH过量,则因过量引起的反应的离子方程式为______________
____________________________________________________。
(3)完成煅烧过程中一个反应的化学方程式:
______CuO+____Al2O3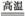 ______CuAlO2+____↑。
______CuAlO2+____↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0 kg废料中的铜可完全转化为________mol CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液____________L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是__________、过滤、洗涤和干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
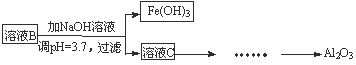
硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%)。某同学设计了如下方案,分离样品中各种金属元素。请回答下列问题。
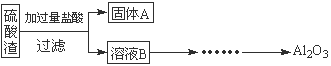
(1)写出溶液B的溶质是 。
(2)参照以下框图形式进一步完成“溶液C”到“Al2O3”的流程(注明试剂、条件和操作) 。
(3)为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定。写出反应的离方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
SiO2、SO2和CO2都是酸性氧化物,它们的化学性质有一定的相似性;Mg和Na的化学性质也有一定相似性。某兴趣小组用如图所示装置进行Mg与SO2反应的实验。
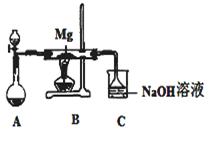
(1)选择制取SO2的合适试剂 (填编号)。
①浓HCl ②浓H2SO4
③Na2SO3固体 ④CaSO3固体
(2)上述装置还可改进,改进的方法是
,
若C中NaOH为0.2mol/L、200ml,通入的SO2为1.12L(标准状况),则该反应的离子方程式为
(3)甲同学推测Mg与SO2的反应与CO2相似,则该反应方程式为
乙同学的推测是:2Mg+3SO2 2MgSO3+S;
2MgSO3+S;
丙同学的推测是:3Mg+SO2 2MgO+MgS,
2MgO+MgS,
要验证甲、乙、丙三位同学的推测是否正确,丁同学作如下实验探究:
已知:MgSO3和MgS都是微溶于水,能与盐酸发生复分解反应放出气体;
限选试剂:2mol/L HCl、2mol/L HNO3、蒸馏水、2mol/L NaOH、品红溶液、澄清石灰水、2mol/L CuSO4;仪器和用品自选。请填写下表中的空格:
根据上述实验探究:
| 序号 | 实验步骤 | 预期现象和结论 |
| ① | 取少量反应后的固体于试管I中 |
|
| ② | 向试管I中的固体慢慢滴加 试管I口塞上带导管的单孔塞,并将导管通入盛有 的试管II中。 | 若试管I中的 , 则丙同学推测正确。若试管I中的固体未完全溶解,且 ,则乙同学的推测正确。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com