
【题目】硼、硅、硒等元素及其化合物用途广泛。请回答下列问题:
(1)基态硒原子的价电子排布式为_______;SeO2常温下为白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体为________晶体。
(2)在硼、硅、硒的气态氢化物中,其立体构型为正四面体的是_______(填化学式),在硅的氢化物中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性大小为Se_____Si(填“>”或“<”)。
(3)在周期表的第二周期中,第一电离能介于硼元素和氮元素之间的元素有_____种。
(4)硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3,BF3·NH3中B与N之间形成______键;NH3中N原子的杂化轨道类型为______,写出与NH3等电子体的一种离子符号________。
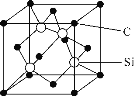
(5)金刚砂(SiC)的摩氏硬度为9.5,其晶胞结构如图所示。在SiC中,每个Si原子周围距离最近的Si原子数目为________;若金刚砂的密度为ρg·cm-3,NA表示阿伏加德罗常数的值,则晶胞中碳原子与硅原子的最近距离为________pm。(用含ρ和NA的式子表示)
【答案】4s24p4 分子 SiH4 > 3 配位 sp3 H3O+ 12 ![]()
【解析】
(1)Se元素为34号元素,原子核外有34个电子,所以核外电子排布式为:1s22s22p63s23p63d104s24p4,基态硒原子的价电子排布式为4s24p4;SeO2常温下白色晶体,熔、沸点低,为分子晶体,故答案为:4s24p4;分子;
(2)硒、硅均能与氢元素形成气态氢化物分别为H2Se,SiH4,其分子结构分别V形、正四面体;若“Si-H”中键合电子偏向氢原子,说明硅显正价,氢气与硒反应时单质硒是氧化剂,硒显负价,所以硒与硅的电负性相对大小为Se>Si,故答案为:SiH4;>;
(3) 第二周期中,元素的第一电离能处于B与N之间的元素有Be、C、O三种,故答案为:3;
(4)BF3NH3中B原子含有3个σ 键和1个配位键,所以其价层电子数是4,B原子采取sp3杂化,该化合物中,B原子提供空轨道的原子、N原子提供孤电子对,所以B、N原子之间形成配位键;在NH3中,N原子的价层电子对数是3+(5-3×1)/2=4,所以杂化轨道类型为sp3;NH3中有10个电子,等电子体的一种离子符号有:H3O+,故答案为:配位;sp3;H3O+;
(5)每个碳原子周围最近的碳原子数目为12,因此在SiC中,每个Si原子周围距离最近的Si原子数目为12;该晶胞中C原子个数=8×![]() +6×
+6×![]() =4,Si原子个数为4,晶胞质量为
=4,Si原子个数为4,晶胞质量为![]() ,设晶胞边长为a pm,则(a×10-10)3×ρ×NA=4×40,解得a=
,设晶胞边长为a pm,则(a×10-10)3×ρ×NA=4×40,解得a=![]() ,碳原子与硅原子的最近距离为晶胞体对角线长度的
,碳原子与硅原子的最近距离为晶胞体对角线长度的![]() ,所以碳原子与硅原子的最近距离为
,所以碳原子与硅原子的最近距离为![]() ,故答案为:12;
,故答案为:12;![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】钻蓝(含Co、Al、O三种元素)是一种带绿光的蓝色颜料。固相法是制备钴蓝颜料方法之一,即将钴、铝的氧化物(或是两者的氢氧化物)按一定比例负载于石墨烯上,然后在马弗炉中高温灼烧、冷却、研磨。回答下列问题:
(1)基态钴原子核外电子排布式为[Ar]__。
(2)下列O原子电子排布图表示的状态中,能量最低的是__(填字母)。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(3)已知Co的活泼性与Fe相近,Co、Al、O的电负性从大到小的顺序为__。
(4)石墨烯的结构如图甲所示。
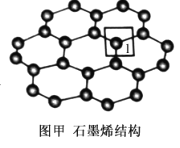
①每个石墨烯分子中,C(如图中1位置处)可形成σ键的个数为__,其杂化类型为___。
②C原子在形成化合物时,其键型以共价键为主,原因是__。
(5)钴蓝晶胞结构如图乙所示,其立方晶胞由4个I型和4个II型小立方体构成。

①钴蓝的化学式为__。
②已知NA为阿伏加德罗常数的值,钴蓝晶体的密度为__g·cm-3(列计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烃B分子内C、H原子个数比为1︰2,相对分子质量为28,核磁共振氢谱显示分子中只有一种化学环境的氢原子,且有如下的转化关系:
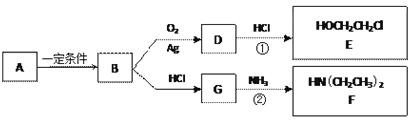
(1)B的结构简式是_________________
(2)A可能属于下列哪类物质___________
a.醇 b.卤代烃 c.酚 d.羧酸
(3)反应①是D与HCl按物质的量之比1︰1的加成反应,则D的分子式是___________。
反应②可表示为:G + NH3→ F + HCl (未配平),该反应配平后的化学方程式是(有机化合物均用结构简式表示): ____________________________________
化合物E(HOCH2CH2Cl)和 F [ HN(CH2CH3)2 ]是药品普鲁卡因合成的重要中间体,普鲁卡因的合成路线如下:(已知:![]() )
)

(4)甲的结构简式是 _________________。
由甲苯生成甲的反应类型是_________________。
(5)乙中有两种含氧官能团,反应③的化学方程式是___________________________________
(6)丙中官能团的名称是_______________________________________。
(7)普鲁卡因有两种水解产物丁和戊。
① 戊与甲互为同分异构体,戊的结构简式是_____________________。
② 戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域。该聚合反应的化学方程式是__________________________________________。
③ D的红外光谱表明分子内除C—H键、C—C键外还含有两个C—O单键。则D与F在一定条件下反应生成丁的化学方程式是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组对人教版教材实验“在200mL烧杯中放入20g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究;
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
其中依据不充分的是_________(填序号);
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:

试回答下列问题:
①图1的A中最好选用下列装置_________(填编号);
②图1的 B装置所装试剂是_________;D装置中试剂的作用是_________;E装置中发生的现象是_________;
③图1的A装置中使蔗糖先变黑的化学反应方程式为_________,后体积膨胀的化学方程式为:_________;
④某学生按图2进行实验时,发现D瓶品红不褪色,E装置中有气体逸出,F装置中酸性高锰酸钾溶液颜色变浅,推测F装置中酸性高锰酸钾溶液颜色变浅的原因_________,其反应的离子方程式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是空气中主要的大气污染物,国家规定在排放前必须经过处理。
Ⅰ.碱液吸收法:工业上常用NaOH溶液做吸收液。
(1)向0.5L1 mol·L-1的NaOH溶液中通入标准状态下11.2L的SO2。
①写出反应的离子方程式__________;
②已知:Ka1=1.54×10-2,Ka2=1.02×10-7,则所得溶液呈_______(填“酸性”、“碱性”或“中性”),下列有关吸收液中粒子浓度大小关系正确的是_________。
A c(H2SO3)>c(SO32-)
B c(Na+)+c(H+)=c(HSO3-)+2c(SO32-)+c(OH-)
C c(Na+)=c(H2SO3)+c(HSO3-)+c(SO32-)
D c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH-)
(2)工业上也可以用Na2SO3溶液吸收SO2,并用电解法处理吸收SO2后所得溶液以实现吸收液的回收再利用,装置如下图所示:

①工作一段时间后,阴极区溶液的pH_______(填“增大”、“减小”或“不变”)。
②写出阳极的电极反应式_______。
Ⅱ.SO2的回收利用:
(3)SO2与Cl2反应可制得磺酰氯(SO2Cl2),反应为SO2(g)+Cl2(g)![]() SO2Cl2(g)。按投料比1:1把SO2与Cl2充入一恒压的密闭容器中发生上述反应,SO2的转化率与温度T的关系如下图所示:
SO2Cl2(g)。按投料比1:1把SO2与Cl2充入一恒压的密闭容器中发生上述反应,SO2的转化率与温度T的关系如下图所示:

① 该反应的ΔH________(填“>”、“<”或“=”)0。
② 若反应一直保持在p压强条件下进行,则M点的分压平衡常数Kp=_____(用含p的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1表示:以相同的滴速分别向同体积的蒸馏水和0.1 mol/L CuSO4溶液中滴入NaCl溶液,氯离子浓度随氯化钠加入量的变化关系。图2表示:CuCl2溶液中氯离子浓度随温度变化关系。结合信息,下列推断不合理的是
已知:CuSO4溶液中存在平衡X:Cu2++4H2O![]() [Cu(H2O)4]2+(蓝色)
[Cu(H2O)4]2+(蓝色)
CuCl2溶液呈绿色,溶液中存在平衡Y:4Cl-+[Cu(H2O)4]2+![]() [CuCl4]2-+4H2O
[CuCl4]2-+4H2O
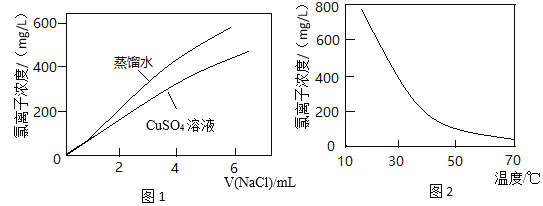
A.平衡Y是图1中两条曲线没有重合的主要原因
B.由图2可知平衡Y为吸热反应
C.平衡X是无水硫酸铜粉末和硫酸铜溶液颜色不同的原因
D.CuCl2溶液加水稀释,溶液最终变为浅绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生物燃料电池原理研究室温下氨的合成,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如下所示。下列说法错误的是

A. 相比现有工业合成氨,该方法条件温和,同时还可提供电能
B. 阴极区,在氢化酶作用下发生反应H2+2MV2+![]() 2H++2MV+
2H++2MV+
C. 正极区,固氮酶为催化剂,N2发生还原反应生成NH3
D. 电池工作时质子通过交换膜由负极区向正极区移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用KOH为电解质的循环阳极锌空气二次电池放电时的总反应为2Zn+O2=2ZnO,工作时,用泵将锌粉与电解液形成的浆料输入电池内部发生反应,反应所生成的产物随浆料流出电池后,被送至电池外部的电解槽中,经还原处理后再送入电池;循环阳极锌-空气二次电池工作流程图如图所示。下列说法错误的是( )
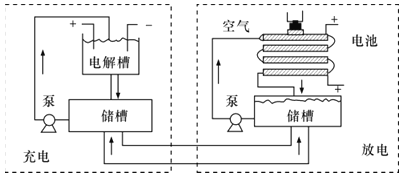
A.放电时,电池正极反应为O2+4e-+2H2O=4OH-
B.放电时,电解质中会生成少量碳酸盐
C.电池停止工作时,锌粉与电解质溶液不反应
D.充电时,电解槽阴极反应为ZnO+2e-+H2O=Zn+2OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com