
分析 (1)氢离子的浓度与盐酸的浓度相等,都是5mol/L;
(2)根据n=cV计算出HCl的物质的量,再根据V=nVm计算出氯化氢的体积.
解答 解:(1)100毫升 5mol•L-1的盐酸溶液中,盐酸为一元强酸,氯化氢完全电离,则溶液中氢离子浓度为5mol/L,
故答案为:5;
(2)100毫升 5mol•L-1的盐酸溶液中含有氯化氢的物质的量为:5mol/L×0.1L=0.5mol,
标准状况下0.5mol氯化氢的体积为:22.4L/mol×0.5mol=11.2L,
故答案为:11.2.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度的概念及表达式为解答关键,注意熟练掌握物质的量与气体摩尔体积、物质的量浓度之间的关系,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 1L0.1mol/L的 Na2S溶液中S2-的个数为0.1NA | |
| B. | 标准状况下,11.2LH2所含的中子数为0.15 NA | |
| C. | 7.8g Na2O2与足量的水反应,转移的电子数为0.2 NA | |
| D. | 1mol羟基所含电子数为9 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )
A、B、C均为短周期元素,它们在周期表中的位置如图.已知B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C所在的一组元素是( )| A. | Be、Na、Al | B. | B、Mg、Si | C. | C、Al、P | D. | O、P、Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2O2(l)=O2(g)+2H2O (l)△H=-196 kJ•mol-1 | |
| B. | 2N2(g)+O2(g)=2N2O(g)△H=+163 kJ•mol-1 | |
| C. | 2Ag(s)+Cl2(g)=2AgCl(s)△H=-254 kJ•mol-1 | |
| D. | 2HgO(s)=2Hg(l)+O2 (g)△H=+182kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50mL 0.50mol/L H2SO4溶液与50mL 0.50mol/L Ba(OH)2溶液 | |
| B. | 50mL 0.50mol/L盐酸溶液与50mL 0.50mol/L NaOH溶液 | |
| C. | 50mL 0.50mol/LCH3COOH溶液与50mL 0.50mol/L NaOH溶液 | |
| D. | 50mL 0.50mol/L盐酸溶液与50mL 0.50mol/L氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
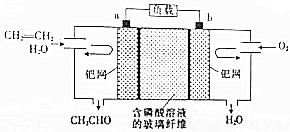
| A. | a极是负极,b极是正极 | |
| B. | 负极的电极反应式为CH2═CH2+H2O+2e-═CH3CHO+2OH- | |
| C. | 当有0.1molO2反应时,会有0.4molH+迁移 | |
| D. | 电子移动方向:电极a→负载→电极b |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 500mL溶液中Cl-离子总数为0.2NA | |
| B. | 500mL溶液中Ba2+和Cl-离子总数为0.3NA | |
| C. | 500mL溶液中Ba2+离子浓度为0.2mol.L-1 | |
| D. | 250mL溶液中Cl-离子浓度为0.2mol.L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com