
下列各组物质不互为同分异构体的是( )
A.2,2二甲基丙醇和 2甲基丁醇
B.邻氯甲苯和对氯甲苯
C.2甲基丁烷和戊烷
D.甲基丙烯酸和甲酸丙酯
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
用“元素符号”填空(前20号元素)
(1)主族序数与周期数相同的元素有________。
(2)主族序数是周期数2倍的元素有________,3倍的元素有________。
(3)周期数是主族序数2倍的元素有________,3倍的元素有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下表信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.氢化物的沸点为H2T<H2R B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
NO分子因污染空气而臭名昭著。近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,成为当前生命科学的研究的热点,NO亦被称为“明星分子”。请回答下列问题:
(1)NO对环境的危害在于________(填以下项目的编号)。
A.破坏臭氧层 B.高温下能使一些金属被氧化
C.造成酸雨 D.与人体血红蛋白结合
(2)在含Cu+的酶的活化中心中,亚硝酸根离子可转化为NO,写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式:_________________________ _______________________________________________。
(3)在常温下,使NO气体压缩到100个大气压,在一个体积固定的容器里加热到50 ℃,发现气体的压力迅速下降,压力降至略小于原压力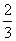 就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式:________________ ______________________________________________________________。
就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式:________________ ______________________________________________________________。
(4)解释变化(3)中为什么最后的气体总压力小于原压力的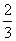 ?
?
_______________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机化合物中,有多个官能团:
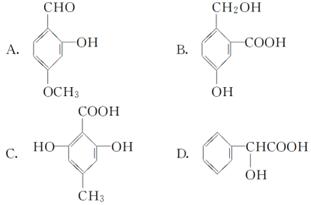
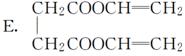
(1)可以看作醇类的是________。(填编号,下同)
(2)可以看作酚类的是________。
(3)可以看作羧酸类的是________。
(4)可以看作酯类的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
判断下列有关烯烃、卤代烃、醇的命名是否正确
(1)CH2===CH—CH===CH—CH===CH2 1,3,5三己烯( )
(2) 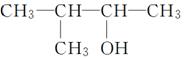 2甲基3丁醇( )
2甲基3丁醇( )
(3) 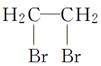 二溴乙烷( )
二溴乙烷( )
(4) 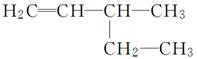 3乙基1丁烯( )
3乙基1丁烯( )
(5) 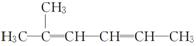 2甲基2,4己二烯( )
2甲基2,4己二烯( )
(6) 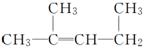 1,3二甲基2丁烯( )
1,3二甲基2丁烯( )
查看答案和解析>>
科目:高中化学 来源: 题型:
对下图两种化合物的结构或性质描述正确的是( )
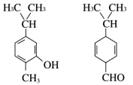
A.不是同分异构体
B.分子中共平面的碳原子数相同
C.均能与溴水反应
D.可用红外光谱区分,但不能用核磁共振氢谱区分
查看答案和解析>>
科目:高中化学 来源: 题型:
化学上常用燃烧法确定有机物的组成。这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。下图所示装置是用燃烧法确定有机物分子式常用的装置。

回答下列问题:
(1)产生的氧气按从左到右流向,所选装置各导管的连接顺序是_________________。
(2)C装置中浓H2SO4的作用是_______________________________________。
(3)D装置中MnO2的作用是________________________________________。
(4)燃烧管中CuO的作用是________________________________________。
(5)若准确称取0.90 g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加1.32 g,B管质量增加0.54 g,则该有机物的最简式为___________________________。
(6)要确定该有机物的分子式,还要___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下。

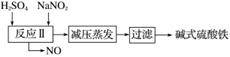
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示。
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题。
(1)加入少量NaHCO3的目的是调节pH,使溶液中的______沉淀,该工艺中“搅拌”的作用是__________。
(2)在实际生产中,反应Ⅱ中常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作________。若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为________。
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+可部分水解生成聚合离子Fe2(OH)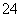 。该水解反应的离子方程式为__________________。
。该水解反应的离子方程式为__________________。
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO 。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母)。
。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母)。
A.氯水 B.KSCN溶液
C.NaOH溶液 D.酸性KMnO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com