
【题目】室温时,CH3COOH的电离平衡常数为K,向20mL 0.1mol/L CH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中正确的是( )

A. b点表示的溶液中c(Na+)>c(CH3COO﹣)
B. c点表示CH3COOH和NaOH恰好反应完全
C. d点表示的溶液中c(CH3COO﹣) c(H+)/c(CH3COOH)大于K
D. b、c、d三点表示的溶液中一定都存在:c(Na+)+c(H+)═c(CH3COO﹣)+c(OH﹣)
科目:高中化学 来源: 题型:
【题目】某同学设计了利用氯酸钾分解制O2测定标准状况下气体摩尔体积的探究实验。
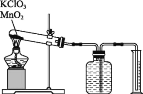
实验步骤如下:①连接好实验装置,检查装置的气密性。②把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95g。③加热,开始反应,直到不再有气体产生为止。④测量排入量筒中水的体积为285.0mL,换算成标准状况下氧气的体积为279.7mL。⑤准确称量试管和残留物的质量为15.55g。根据上述实验过程,回答下列问题。
(1)如何检查装置的气密性?________。
(2)以下是测量收集到的气体体积必须包括的几个步骤:①使试管和广口瓶内气体都冷却至室温;②_____;③读取量筒内液体的体积。进行③的实验操作时,若仰视读数,则读取氧气的体积__ (填“偏大”“偏小”或“无影响”)。
(3)实验过程中产生氧气的物质的量是______mol;实验测得标准状况下氧气的摩尔体积是__ (保留小数点后两位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中通常伴随着能量变化,下列说法中错误的是( )
A. 煤燃烧时将部分化学能转化为热能B. 电解熔融Al2O3时将部分化学能转化为电能
C. 炸药爆炸时将部分化学能转化为动能D. 镁条燃烧时将部分化学能转化为光能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的是( )
A. 用 所示装置分离CCl4和I2的混合物
所示装置分离CCl4和I2的混合物
B. 用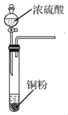 所示装置获取少量SO2气体
所示装置获取少量SO2气体
C. 用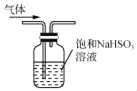 所示装置除去CO2气体中的少量SO2
所示装置除去CO2气体中的少量SO2
D. 用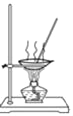 所示装置蒸发NaCl溶液获得NaCl晶体
所示装置蒸发NaCl溶液获得NaCl晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s)![]() NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
2NO(g)+Cl2(g)![]() 2NOCl(g) K2 ΔH2<0 (Ⅱ)
2NOCl(g) K2 ΔH2<0 (Ⅱ)
(1)4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________(用K1、K2表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________(用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(NOCl)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=________ mol,NO的转化率α1=________。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2________α1(填“>”“<”或“=”),平衡常数K2________(填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是____________。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2 +2NaOH =NaNO3 +NaNO2 +H2O。含0.2 mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1 mol/L的CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-)和c(CH3COO-)由大到小的顺序为_______________。(已知HNO2的电离常数Ka=7.1×10-4 mol/L,CH3COOH的电离常数Ka=1.7×10-5 mol/L)可使溶液A和溶液B的pH相等的方法是_____。
a.向溶液A中加适量水
b.向溶液A中加适量NaOH
c.向溶液B中加适量水
d.向溶液B中加适量NaOH
(Ⅱ)在恒压密闭容器中,充入一定量的H2和CO2 发生如下可逆反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH<0,实验测得反应物在不同温度下,反应体系中CO2的平衡转化率与压强的关系曲线如图所示。
CH3OH(g)+H2O(g)ΔH<0,实验测得反应物在不同温度下,反应体系中CO2的平衡转化率与压强的关系曲线如图所示。
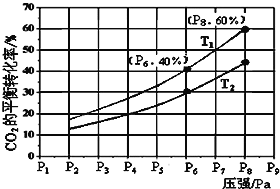
(1)该反应的ΔS______0(填>或<),该反应在_______(填“低温”或“高温”)条件下利于自发进行;
(2)比较T1与T2的大小关系:T1__T2(填“<”、“=”或“>”),理由是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A. 常温常压下,11.2L二氧化硫所含的氧原子数等于NA
B. 0.5molH2O所含的电子数为9NA
C. 8.0gCu2S和CuO的混合物中含有铜原子数为0.1NA
D. 300mL2mol·L-1蔗糖溶液中所含分子数为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】欲用Na2CO3固体配制950mL 0.1 mol·L-1的Na2CO3溶液。配制过程如下图所示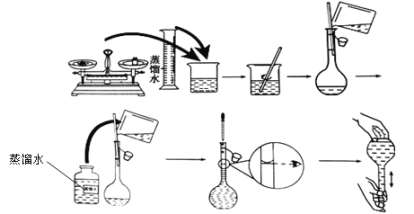
请根据题意回答:
(1)配制该溶液应选用__________mL容量瓶。
(2)用托盘天平称取_________g固体Na2CO3固体。
(3)向容量瓶中加入蒸馏水,直到液面在刻度线下1~2cm时,改用____________滴加蒸馏水至液面的最低点与刻度线相切,盖好瓶塞,摇匀。
(4)在配制上述溶液的实验中,下列操作中会引起结果偏低的有____________(填序号)
A.在烧杯中搅拌溶解溶质时,溅出少量溶液
B.未将洗涤烧杯内壁的溶液转移至容量瓶
C.定容时,加水超过了刻度线,倒出一些再重新加水至刻度线
D.将所配溶液从容量瓶转移到试剂瓶时有少量溶液溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗铜精炼后的阳极泥中含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的工艺流程如图所示:

(1)电解精炼含铜、金、铅的粗铜时,电解液应该用________溶液作电解液,电解时阳极的电极反应式为___________________________和Cu-2e-===Cu2+。
(2)完成操作Ⅰ的主要步骤有:__________________,过滤,洗涤,干燥。
(3)写出用SO2还原AuCl4-的离子反应方程式____________________________。
(4)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法________________________。
(5)用离子方程式表示加入碳酸钠溶液的作用:___________________________。[已知298 K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)=1.82×10-8]。当溶液中c(SO42-)=0.2mol/L时,c(CO32-)=_______________mol/L。(结果保留2位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com