
| A. |  1,3,4-三甲苯 1,3,4-三甲苯 | B. |  2-甲基戊烷 2-甲基戊烷 | ||
| C. |  2-甲基-1-丙醇 2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 2-甲基-3-丁炔 |
分析 (1)烷烃命名原则:
①长-----选最长碳链为主链;
②多-----遇等长碳链时,支链最多为主链;
③近-----离支链最近一端编号;
④小-----支链编号之和最小.看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简-----两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面.
(2)有机物的名称书写要规范;
(3)对于结构中含有苯环的,命名时可以依次编号命名,也可以根据其相对位置,用“邻”、“间”、“对”进行命名;
(4)含有官能团的有机物命名时,要选含官能团的最长碳链作为主链,官能团的位次最小.
解答 解:A.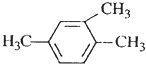 1,3,4-三甲苯,该命名中取代基的编号之和不是最小,正确命名应该为:1,2,4-三甲苯,故A错误;
1,3,4-三甲苯,该命名中取代基的编号之和不是最小,正确命名应该为:1,2,4-三甲苯,故A错误;
B. 主链有5个碳原子的烷烃,2号碳上有1个甲基,其名称为:2-甲基戊烷,故B正确;
主链有5个碳原子的烷烃,2号碳上有1个甲基,其名称为:2-甲基戊烷,故B正确;
C. 主链为4个碳原子的醇,羟基在2号碳原子上,其名称为:2-丁醇,故C错误;
主链为4个碳原子的醇,羟基在2号碳原子上,其名称为:2-丁醇,故C错误;
D. 主链为4个碳的炔,碳碳三键在1号碳上,3号碳上有1个甲基,其名称为:3-甲基-1-丁炔,故D错误;
主链为4个碳的炔,碳碳三键在1号碳上,3号碳上有1个甲基,其名称为:3-甲基-1-丁炔,故D错误;
故选:B.
点评 本题考查了考查有机物的命名,侧重对学生基础知识的检验和训练,该题的关键是明确有机物的命名原则,然后结合有机物的结构简式灵活运用即可,有利于培养学生的规范答题能力.


科目:高中化学 来源: 题型:选择题

| A. | 试剂M 是HBr,加入HBr的目的是除去过量的Ca(OH)2 | |
| B. | 操作I为过滤,滤渣为Fe、Fe(OH)2和Fe(OH)3;操作Ⅱ为重结晶,具体操作步骤为蒸发浓缩、冷却结品、洗涤、干燥 | |
| C. | 制得的CaBr2•2H2O 可以通过以下方法测定纯度:称取一定量的样品溶于水,滴入足量Na2CO3溶液,充分反应后过滤,将滤渣洗涤、烘干、冷却、称量,计算便得出CaBr2•2H2O的纯度 | |
| D. | 工业上也可以将氨气通入石灰乳,并加入溴,于65℃进行反应,制得溴化钙,此反应中还会生成一种无色气体,该反应的化学方程式为3Ca(OH)2+3Br2+2NH3$\frac{\underline{\;\;△\;\;}}{\;}$3CaBr2+N2+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A是气体 | B. | B是气体 | ||
| C. | 如果C是气体,A、B一定是气体 | D. | 如果C是气体,B不一定是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | ① | ② | ③ | ④ |
| 科学家 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
| 工作 | 发现“八音律”,指出从某一指定的元素起,第八个元素是第一个元素的某种重复 | 创立近代原子论,率先开始相对原子质量的测定工作 | 发现了5组性质相似的“三元素组”,中间元素的相对原子质量为前后两种元素相对原子质量的算术平均值 | 认为各元素组之间并非毫不相关,可以用相对原子质量把它们按从小到大的顺序串联 |
| Ni=Co=59 | |||||
| H=1 | Cu=63.4 | Ag=108 | Hg=200 | ||
| Be=9.4 | Mg=24 | Zn=65.2 | Cd=112 | ||
| B=11 | Al=27.4 | ?=68 | Ur=116 | Au=198? | |
| C=12 | Si=28 | ?=70 | Sn=118 | ||
| N=14 | P=31 | As=75 | Sb=122 | Bi=210? | |
| O=16 | S=32 | Se=79.4 | Te=128? | ||
| F=19 | Cl=35.5 | Br=80 | I=127 | ||
| Li=7 | Na=23 | K=39 | Rb=85.4 | Cs=133 | Tl=204 |
| Ca=40 | Pb=207 |
 ,元素Z的离子结构示意图为
,元素Z的离子结构示意图为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳、苯和乙醇均能用来萃取富集天然色素 | |
| B. | 用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏 | |
| C. | 在苯甲酸重结晶的实验中,苯甲酸停留在滤纸上 | |
| D. | 在苯甲酸重结晶的实验中,粗苯甲酸完全溶解后要冷却到常温才过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫酸工业在国民经济中占有极其重要的地位.
硫酸工业在国民经济中占有极其重要的地位.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
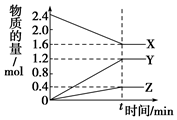 一定温度下,在0.5L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,10s时达到化学平衡状态.下列说法正确的是( )
一定温度下,在0.5L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,10s时达到化学平衡状态.下列说法正确的是( )| A. | 该反应的化学方程式为:2X?3Y+Z | |
| B. | 10s内Y的平均速率为0.12 mol•L-1•min-1 | |
| C. | X的转化率为66.7% | |
| D. | 增大压强,该反应速率一定加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ④CH3CH3.
④CH3CH3.| A. | ①② | B. | ③④ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com