
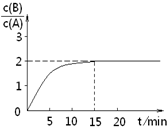
 ̉ÑÖª£¬Ä³Î¶ÈÏÂÔÚ2LĂܱƠÈƯÆ÷ÖĐ¼ÓÈë̉»¶¨Á¿A£¬·¢Éú̉ÔÏ»¯Ñ§·´Ó¦£º
̉ÑÖª£¬Ä³Î¶ÈÏÂÔÚ2LĂܱƠÈƯÆ÷ÖĐ¼ÓÈë̉»¶¨Á¿A£¬·¢Éú̉ÔÏ»¯Ñ§·´Ó¦£º| A¡¢·´Ó¦ÔÚÇ°15minµÄƽ¾ùËÙÂʦͣ¨A£©=0.11 mol?L-1?min-1 | B¡¢AµÄ³ơʼÎïÖʵÄÁ¿Îª8 mol | C¡¢·´Ó¦µ½´ïƽºâµÄ¹ư³̀ÖĐ£¬·Å³öµÄÈÈÁ¿ÊÇ77.2kJ | D¡¢Èçʹ·´Ó¦×îÖƠc£¨B£©/c£¨A£©=1.5£¬ºăκăÈƯʱ£¬¼ÓÈë̉»¶¨Á¿µÄA¿É̉ÔʵÏÖ |
| c(B) |
| c(A) |
| ¡÷C |
| ¡÷t |
| c(B) |
| c(A) |
| c(B) |
| c(A) |
| 3.2mol?L-1 |
| 15min |
| 6.4mol |
| 2mol |
| c(B) |
| c(A) |


 Ăûʦµă¾¦×ִʾä¶ÎƪϵÁĐ´đ°¸
Ăûʦµă¾¦×ִʾä¶ÎƪϵÁĐ´đ°¸
| Ä꼶 | ¸ßÖĐ¿Î³̀ | Ä꼶 | ³ơÖĐ¿Î³̀ |
| ¸ß̉» | ¸ß̉»Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ở» | ³ở»Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ß¶₫ | ¸ß¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ | ³ơ¶₫ | ³ơ¶₫Ăâ·Ñ¿Î³̀ÍƼö£¡ |
| ¸ßÈư | ¸ßÈưĂâ·Ñ¿Î³̀ÍƼö£¡ | ³ơÈư | ³ơÈưĂâ·Ñ¿Î³̀ÍƼö£¡ |
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£ºÔĶÁÀí½â
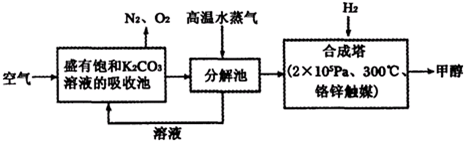
| ÎïÖÊ | H2 | CO | CH3OH |
| Ũ¶È/£¨mol?L-1£© | 0.2 | 0.2 | 0.4 |
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
 ̉ÑÖª£¬Ä³Î¶ÈÏÂÔÚ2LĂܱƠÈƯÆ÷ÖĐ¼ÓÈë̉»¶¨Á¿A£¬·¢Éú̉ÔÏ»¯Ñ§·´Ó¦£º
̉ÑÖª£¬Ä³Î¶ÈÏÂÔÚ2LĂܱƠÈƯÆ÷ÖĐ¼ÓÈë̉»¶¨Á¿A£¬·¢Éú̉ÔÏ»¯Ñ§·´Ó¦£º| A¡¢¸ĂζÈÏ´˷´Ó¦Æ½ºâ³£ÊưΪ3.2 | B¡¢AµÄ³ơʼÎïÖʵÄÁ¿Îª4 mol | C¡¢·´Ó¦µ½´ïƽºâµÄ¹ư³̀ÖĐ£¬·Å³öµÄÈÈÁ¿ÊÇ154.4kJ | D¡¢Èçʹ·´Ó¦×îÖƠc£¨B£©/c£¨A£©=3£¬Ö»ÄܽµµÍ·´Ó¦ÎÂ¶È |
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º2012-2013ѧÄê±±¾©ÊĐ·¿É½Çø¸ßÈưµÚ¶₫´ÎÄ£Ä⻯ѧÊÔ¾í£¨½âÎö°æ£© ̀âĐÍ£ºÑ¡Ôñ̀â
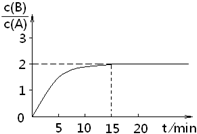
̉ÑÖª£¬Ä³Î¶ÈÏÂÔÚ2LĂܱƠÈƯÆ÷ÖĐ¼ÓÈë̉»¶¨Á¿A£¬·¢Éú̉ÔÏ»¯Ñ§·´Ó¦£º2A(g) 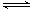 B(g)+C(g)£»¦¤H =-48.25 kJ
¡¤ mol£1·´Ó¦¹ư³̀ÖĐʱ¼ätÓëA ¡¢BŨ¶ÈÓĐÏÂͼËùʾ¹Øϵ£¬Èô²âµĂµÚ15minʱc(B)=1.6 mol¡¤L£1£¬ỘÏÂÁĐ½áÂÛƠưÈ·µÄÊÇ
B(g)+C(g)£»¦¤H =-48.25 kJ
¡¤ mol£1·´Ó¦¹ư³̀ÖĐʱ¼ätÓëA ¡¢BŨ¶ÈÓĐÏÂͼËùʾ¹Øϵ£¬Èô²âµĂµÚ15minʱc(B)=1.6 mol¡¤L£1£¬ỘÏÂÁĐ½áÂÛƠưÈ·µÄÊÇ

A£®¸ĂζÈÏ´˷´Ó¦Æ½ºâ³£ÊưΪ3.2
B£®AµÄ³ơʼÎïÖʵÄÁ¿Îª4 mol
C£®·´Ó¦µ½´ïƽºâµÄ¹ư³̀ÖĐ£¬·Å³öµÄÈÈÁ¿ÊÇ154.4kJ
D£®Èçʹ·´Ó¦×îÖƠc(B)/c(A)=3£¬Ö»ÄܽµµÍ·´Ó¦Î¶È
²é¿´´đ°¸ºÍ½âÎö>>
¿ÆÄ¿£º¸ßÖĐ»¯Ñ§ À´Ô´£º ̀âĐÍ£º
̉ÑÖªºÏ³É°±·´Ó¦N2£¨g£©+3H2£¨g£©![]() 2NH3£¨g£©¡÷H£½£92.30kJ ¡¤mol£1£¬ÔÚijζÈÏ£¬2LµÄĂܱƠÈƯÆ÷ÖĐ½øĐĐ£¬²âµĂÈçÏÂÊư¾Ư£º
2NH3£¨g£©¡÷H£½£92.30kJ ¡¤mol£1£¬ÔÚijζÈÏ£¬2LµÄĂܱƠÈƯÆ÷ÖĐ½øĐĐ£¬²âµĂÈçÏÂÊư¾Ư£º
¡¡ 
ÏÂÁĐ˵·¨ƠưÈ·µÄÊÇ
A£®·´Ó¦½øĐе½1Đ¡Ê±Ê±·Å³öµÄÈÈÁ¿Îª9.23kJ
B£®·´Ó¦3hÄÚ£¬·´Ó¦ËÙÂÊv£¨N2£©Îª0.17mol¡¤L£1¡¤h£1
C£®´ËζÈÏ£¬¸Ă·´Ó¦µÄƽºâ³£ÊưΪ0.037
D£®4hʱ£¬ÈôÔÙ¼ÓÈë1mol N2£¬´ïµ½ĐµÄƽºâʱ£¬N2µÄת»¯ÂÊÊÇÔÀ´µÄÁ½±¶
²é¿´´đ°¸ºÍ½âÎö>>
°Ù¶ÈÖÂĐÅ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com