
【题目】BHT是一种常用的食品抗氧化剂,从![]() 出发合成BHT的方法有如下两种。下列说法不正确的是( )
出发合成BHT的方法有如下两种。下列说法不正确的是( )
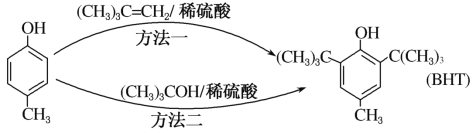
A. 方法一和方法二的反应类型都是加成反应
B. BHT与![]() 都能使酸性KMnO4溶液褪色
都能使酸性KMnO4溶液褪色
C. 推测BHT在水中的溶解度小于苯酚
D. BHT与![]() 互为同系物
互为同系物
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列装置(部分夹持装置及石棉网已省略)或操作能达到实验目的的是
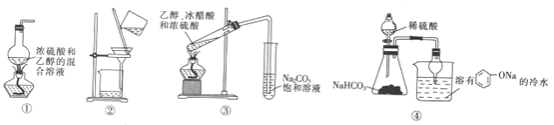
A. 用装置①制乙烯B. 用装置②分离苯和苯酚
C. 用装置③制备乙酸乙酯D. 用装置④验证硫酸、碳酸、苯酚酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向25 mL 0.1 mol·L-1NaOH溶液中逐滴滴加0.2 mol·L-1的HN3(叠氮酸)溶液,pH的变化曲线如图所示(溶液混合时体积的变化忽略不计,叠氮酸的是一元弱酸)。下列说法正确的是
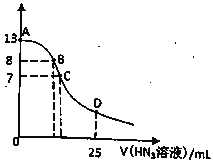
A. 在C点,滴加的V(HN3)=12.5 mL
B. 在B点,离子浓度大小为 c(OH-)>c(H+)>c (Na+)>c(N3-)
C. 水电离出的c(H+):A点小于B点
D. 在D点,c(Na+)=2c(HN3)+2 c(N3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在给定条件下一定能大量共存的是
A. 强酸性溶液中:H+、NO3-、SO32-
B. pH=12的溶液中:OH-、K+、Cl-、HCO3-
C. 加入铝粉能放出氢气的溶液中一定存在:NH4+、NO3-、AlO2-、SO42-
D. 25C时pH=7的无色溶液中:Na+、Cl-、SO42-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示。

(1)其负极是_________(填“Zn”或“Cu”),发生的是__________(填“氧化”或“还原”)反应,电极反应式为___________________ 。
(2)正极上的现象是________________________________________。
(3)电子由_______________(填“锌片”或“铜片”)沿导线流出。
(4)电池总反应的离子方程式是_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年5月美国研究人员成功实现在常温常压下用氮气和水生产氨,原理如下图所示:
下列说法正确的是( )
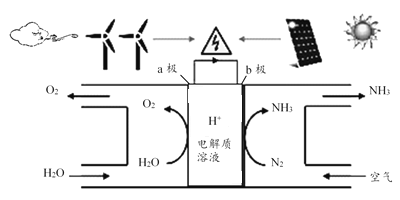
A. 图中能量转化方式只有2种
B. H+向a极区移动
C. b极发生的电极反应为:N2+6H++6e-=2NH3
D. a极上每产生22.4LO2流过电极的电子数一定为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后生成的气体的体积比为甲∶乙=1∶2,则加入铝粉的质量为( )
A.5.4 gB.3.6 gC.2.7 gD.1.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】泄盐(MgSO4·7H2O)是一种中药药剂,还可用于制革、肥料、瓷器、印染料等工业。一种利用氯碱工业的废渣(主要成分是Mg(OH)2,杂质为MnCO3、FeCO3、Al(OH)3、SiO2等)生产泄盐的流程如下:

已知部分氢氧化物沉淀pH如下表:
氢氧化物 | Fe(OH)3 | Mg(OH)2 | Al(OH)3 | Al(OH)3在pH=7.8时开始溶解,pH=10.0完全溶解 |
开始沉淀的pH | 2.3 | 10.8 | 3.7 | |
完全沉淀的pH | 4.3 | 12.4 | 5.2 |
回答下列问题:
(1) “酸浸”是工业对矿物利用的一种方法,该操作关键是提供浸取率和浸取速率,写出提高该工艺流程中“酸浸”速率的2种方法:___________________。
(2) “操作1” “操作2”和“操作3”相同,实验室在进行该操作时,用到的玻璃仪器有________,“滤渣1”的成分是________(写化学式)。
(3) “氧化(煮沸)”操作的目的是使溶液中的锰元素转化为MnO2,写出该反应的离子方程式:____________________。
(4)“调节pH”时最好选用__________, pH范围应控制为____________,高温加热“滤渣3”可得到_________(写化学式)。
(5) “一系列操作”是指_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铅酸蓄电池的工作原理如图所示,其总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。下列判断不正确的是( )
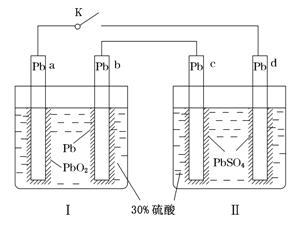
A. 闭合K时,d电极的反应式为PbSO4+2H2O-2e-=PbO2+4H++SO42—
B. 当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol
C. 闭合K时,Ⅱ中SO42—向c电极迁移
D. 闭合K一段时间后,Ⅱ可单独作为原电池,d电极为正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com