
【题目】常见物质A~K之间存在如下图所示的转化关系,其中D、E为单质,请回答下列问题(图中有些反应的产物和反应的条件没有全部标出)。

(1)写出下列物质中溶质的名称:B是 __________,G是____________
(2)反应“F→G”的化学方程式是_____________________________________________
(3)反应“J→I”的离子方程式是_____________________________________________
(4)溶液I中混有溶液J,除去J的方法是:________________________________________________________________
(5)检验溶液I中阳离子的方法是:__________________________
【答案】 氯化氢 偏铝酸钠 Al(OH)3+NaOH=NaAlO2+2H2O 2Fe3++Fe=3Fe2+ 加入足量的铁粉(过滤) 取少量溶液I于试管中,滴加几滴硫氰化钾溶液,溶液不变红色,再加几滴氯水,溶液变为红色,证明溶液中含有Fe2+。
【解析】C中加氨水生成白色沉淀F,F可溶于NaOH溶液中,可知F为Al(OH )3,则C中含有Al3+,从而A为Al。E为Cl2,D为气体且与Cl2反应生成另一种气体B,可推测B为HCl。验证可知B确为HCl。由红褐色沉淀K可知K为Fe(OH)3,所以H为Fe。
(1)由上面分析可知B是氯化氢、F为Al(OH )3,与NaOH反应生成Na2AlO2,G的名称为偏铝酸钠。
(2)Al(OH )3与NaOH反应生成Na2AlO2和H2O,化学方程式为:Al(OH)3+NaOH=NaAlO2+2H2O。
(3)金属H为Fe,B为HCl,所以I为FeCl2,J为 FeCl3,J→I的离子方程式为:2Fe3++Fe=3Fe2+。
(4)FeCl2溶液中混有FeCl3,可加入足量的Fe粉使Fe3+转化为Fe2+,然后过滤。
(5)检验FeCl2中Fe2+的方法:取少量溶液I于试管中,滴加几滴硫氰化钾溶液,溶液不变红色,再加几滴氯水,溶液变为红色,证明溶液中含有Fe2+。


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】取一定质量的氯化钠、溴化钠、碘化钠的混合物平均分成五等份,分别加水配成溶液并编号为甲、乙、丙、丁、戊,再分别向各溶液中通入一定体积的氯气,将反应后所得溶液蒸干,灼烧固体。通入氯气的量与最终所得固体质量记录如下:
编号 | 甲 | 乙 | 丙 | 丁 | 戊 |
固体组成 | NaI、NaBr、NaCl | NaBr、NaCl | NaCl | ||
氯气的体积/ml | V | 2V | 3V | 4V | 5V |
固体质量/g | 54.62 | 43.64 | 35.48 | 30.14 | 29.25 |
求:(1)请填写表中空白______________、____________;
(2)标准状况下氯气的体积V为_______,原混合物中溴化钠的物质的量为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,学好化学终生有益。如人体正常的血红蛋白中含有Fe2+,若误食NaNO2,则使血红蛋白中Fe2+转化为Fe3+而丧失其生理功能,临床证明服用维生素C可以解毒,这说明维生素C 具有
A. 酸性 B. 碱性 C. 还原性 D. 氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制Cl2反应为4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O,下列说法不正确的是
MnCl2+Cl2↑+2H2O,下列说法不正确的是
A. 还原剂是HCl,氧化剂是MnO2
B. 每生成1mol Cl2,转移电子的物质的量为2mol
C. 每消耗1mol MnO2,起还原剂作用的HCl消耗4mol
D. 转移电子的物质的量为1mol时,生成标准状况下Cl2的体积为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分散系最不稳定的是
A. 向NaOH溶液中通入CO2得到的无色溶液
B. 向碘水溶液中滴加四氯化碳充分振荡后,静置后的下层液体
C. 向沸水中滴入饱和的FeCl3溶液得到的红褐色液体
D. 向CuSO4溶液中加入NaOH溶液得到的分散系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为元素周期表的一部分.
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题:
(1)Z元素在周期表中的位置为 .
(2)表中元素原子半径最大的是(填元素符号) .
(3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是 . a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
(4)沸点:H2YH2S(填“>”或“=”或“<”),理由是 .
(5)Y2和Y3互为(填“同位素”或“同分异构体”或“同素异形体”).
(6)其中单质Y2可用做如图所示装置(燃料电池)的氧化剂,请写出Y2在酸性电解质溶液中发生的电极反应方程式 . 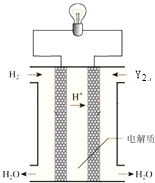
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学常见物质间的转化关系图(部分反应条件、产物已省略),G为铝,A 为日常生活中的常见金属。常温下,B、C、E、H、I、J 为气体,C 为黄绿色气体,M 为红褐色胶体。
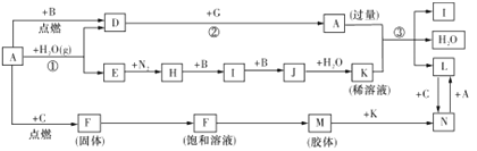
(1)A的元素名称为_________。
(2)D 与G 在高温下反应生成A单质和G的氧化物,请写出其化学方程式:__________。
(3)请写出反应③ 的离子方程式:__________。
(4)请写出H→I的化学方程式:__________。
(5)现将一试管J 气体倒立于水槽中一段时间后,水面上升但不充满;若要使水充满整个试管.应向试管内通入一定量_____(填气体的化学式),此时试管内溶液中溶质的物质的量浓度为_____(气体体积按标准状况计算)(保留两位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com