
【题目】已知:①C2H6(g)![]() C2H4(g)+H2(g) H1 >0。
C2H4(g)+H2(g) H1 >0。
②C2H6(g)+![]() =2CO2(g)+3H2O(l) H 2 =-1559.8 kJ·mol-1
=2CO2(g)+3H2O(l) H 2 =-1559.8 kJ·mol-1
③C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) H 3=-1411.0 kJ·mol-1
下列叙述正确的是
A.升温或加压均能提高①中乙烷的转化率
B.①中断键吸收的能量少于成键放出的能量
C.用H 2和H 3可计算出①中的H
D.推测1 mol C2H2(g)完全燃烧放出的热量小于1411.0 kJ
科目:高中化学 来源: 题型:
【题目】某工厂废金属屑的主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该工厂的金属废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。

完成下列填空:
(1)写出步骤Ⅰ反应的离子方程式:___。
(2)试剂X是___,溶液D是___。
(3)在步骤Ⅱ中,用如图装置制取CO2并通入溶液A中。一段时间后,仍观察不到烧杯中产生白色沉淀。为了固体C的生成,在药品和装置上可采取的改进措施是___。
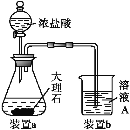
(4)溶液E中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+,用离子方程式解释其可能的原因:___。
(5)将固体F继续加入热的稀硫酸,同时不断鼓入空气,固体溶解得CuSO4溶液,写出反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯是重要的有机化工原料。以下是丙烯合成F的路线(反应条件及无机产物忽略)。、
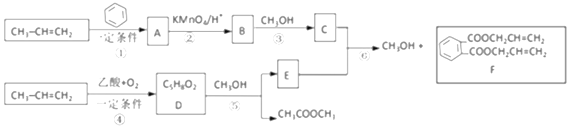
已知:①![]() +2CH2=CH2
+2CH2=CH2![]()
![]() 或
或![]()
②一定条件下,脂与醇会发生交换反应:RCOOR′+R"OH![]() RCOOR"+R′OH
RCOOR"+R′OH
③![]()
![]()
![]()
(1)反应①的反应类型是________反应;由反应①生成的A有______种可能的结构,这些不同结构的A在酸性高锰酸钾作用下都得到B。反应①还会生成A的一种同分异构体M。M中有3种化学环境不同的氢,则M的结构简式为_________。
(2)写出D的结构简式______,E中官能团的名称_____。
(3)写出反应⑥的化学方程式____________。
(4)写出以丙烯为原料制备甘油的流程图__________(其他原料任选,可选用提目中提供的信息)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的几种离子,已知各离子的浓度均相等,进行如下实验:
中的几种离子,已知各离子的浓度均相等,进行如下实验:
![]() 取少量该溶液,加入足量稀硫酸,无明显现象。
取少量该溶液,加入足量稀硫酸,无明显现象。
![]() 取
取![]() 反应后的溶液,加入足量浓NaOH溶液,最终得到红褐色沉淀,并伴有刺激性气味气体产生。下列说法不正确的是
反应后的溶液,加入足量浓NaOH溶液,最终得到红褐色沉淀,并伴有刺激性气味气体产生。下列说法不正确的是![]()
![]()
A.该溶液中肯定不存在![]() 、
、![]() 、
、![]()
B.另取该溶液,加入适量氯水和淀粉溶液,若溶液显蓝色,即可确定该溶液中一定不含![]()
C.取原溶液进行焰色反应,显黄色,则溶液中一定含有的离子有六种
D.该溶液中肯定存在![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示是中学化学中常用于混合物分离和提纯的装置:
A 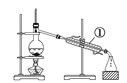 B
B 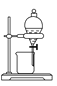 C
C 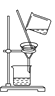 D
D 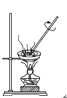
请根据装置图回答下列问题:
(1)从氯化钾溶液中得到氯化钾固体选择装置______(填代表装置图的字母,下同);除去自来水中的Cl-等杂质得到蒸馏水,选择装置_____。
(2)从碘水中分离出I2,选择装置____,该分离方法的名称为________。
(3)装置A中①的名称是________,冷凝水流动的方向是__________。
(4)分液时要注意及时________,防止上层液体流下。分液后漏斗内剩余的液体从分液漏斗的________(填“上口”或“下口”)倒入烧杯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D是四种短周期元素,E是过渡元素。A,B,C同周期,C,D同主族,A的原子结构示意图为 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的符号:A________,B________,C________,D________。
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是________,碱性最强的是__________。
(3)用元素符号表示D所在周期第一电离能最大的元素是________,电负性(除稀有气体外)最大的元素是_________。
(4)E元素原子的核电荷数是_________,E元素在周期表的第_______周期第_______族,在________区。
(5)写出D元素原子构成单质的电子式___________,该分子中有_______个σ键,_______个π键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色植物标本用醋酸铜[(CH3COO)2Cu]处理后颜色更鲜艳、稳定。某化学小组制备醋酸铜晶体并测定产品中铜的含量,实验如下。
Ⅰ.醋酸铜晶体的制备

(1)①中,用离子方程式表示产物里OH-的来源是__________。
(2)②中,化学方程式是__________。
(3)③中采用的实验方法依据醋酸铜的性质是_________。
Ⅱ.测定产品中铜的含量
ⅰ.取a g醋酸铜产品于具塞锥形瓶中,用稀醋酸溶解,加入过量KI溶液,产生CuI沉淀,溶液呈棕黄色;
ⅱ.用b molL-1 Na2S2O3标准溶液滴定ⅰ中的浊液至浅黄色时,加入几滴淀粉溶液,溶液变蓝,继续用Na2S2O3标准溶液滴定至蓝色近于消失;
ⅲ.向ⅱ所得浊液中加入KSCN溶液,充分摇动,溶液蓝色加深;
ⅳ.继续用Na2S2O3 标准溶液滴定ⅲ中浊液至终点,消耗标准溶液v mL。
已知:①![]() ,Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
,Na2S2O3溶液和Na2S4O6溶液颜色均为无色;
②CuI易吸附I2,CuSCN难溶于水且不吸附I2。被吸附的I2不与淀粉显色。
(4)ⅰ中发生反应的离子方程式是__________。
(5)结合离子方程式说明,ⅲ中加入KSCN的目的是__________。
(6)醋酸铜产品中铜元素的质量分数是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己酮(![]() )在生产生活中有重要的用途,可在酸性溶液中用环己醇间接电解氧化法制备,其原理如图所示。下列说法正确的是
)在生产生活中有重要的用途,可在酸性溶液中用环己醇间接电解氧化法制备,其原理如图所示。下列说法正确的是
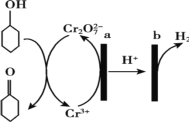
A.a 极与电源负极相连
B.a 极电极反应式是 2Cr3+- 6e- +14OH-= Cr2O72-+7H2O
C.b 极发生氧化反应
D.理论上生成 1mol 环己酮时,有 1molH2 生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com