
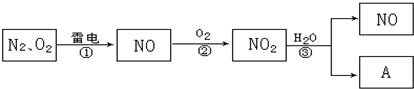


科目:高中化学 来源: 题型:
A、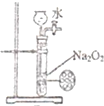 制备少量的氧气 |
B、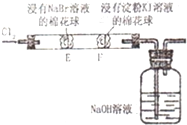 证明氧化性Cl2>Br2>I2 |
C、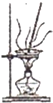 将海带灼烧成灰 |
D、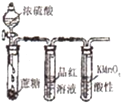 说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、脂肪 | B、乙酸 |
| C、葡萄糖 | D、蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、达平衡时,SO2的消耗速率必定等于O2的生成速率的2倍 |
| B、达平衡时,升高温度,逆反应速率增加,正反应速率减小 |
| C、达平衡后,若保持压强不变,充入少量氖气,则平衡向左移 |
| D、达平衡后,若保持体积不变,充入少量O2气体,则平衡向右移,SO2转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气生成 |
| B、将除去氧化膜的相同大小、相同质量的镁条和铝条与相同浓度盐酸反应,前者速率大于后者 |
| C、两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
| D、相同条件下等质量的块状和粉末状大理石与相同浓度盐酸反应时,粉末状的反应速率快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向蔗糖中加入浓硫酸后出现发黑现象,说明浓H2SO4具有脱水性 |
| B、浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 |
| C、稀释浓硫酸时应将水沿着烧杯壁慢慢地注入盛有浓硫酸的烧杯中,并不断搅拌 |
| D、硝酸常温下能与铜反应,说明硝酸有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1的溶液中:Na+、I-、NO3-、SO42- |
| B、氢氧化铁胶体中:H+、K+、Cl-、S2- |
| C、在pH=0的溶液中:Na+、NH4+、NO3-、Cl- |
| D、水电离产生的c(H+)=1×10-12mol?L-1的溶液中:HCO3-、NH4+、Cl-、Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 | ||||||||
| 周期 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ | Ⅶ | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com