
ʳƷ���Ӽ��������һ���㾫����ϳ�·�����£�
��ش��������⣺
(1)A��C�����¶�����ɫ����ˮ��Һ�壬�����߽��м�����Լ��� ��
(2)�����仯��������ȥ��Ӧ���� (�Ӧ���)��
(3)E�Ľṹ��ʽΪ ��
д����Ӧ�ڵĻ�ѧ��Ӧ����ʽ ��
(4)ͬʱ��������Ҫ���������ͬ���칹���� ��(�����������)��д������һ�ֵĽṹ��ʽ ��
I�����б��� II������NaHCO3��Һ��Ӧ III����ʹ������Ȼ�̼��Һ��ɫ
 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ͼװ����ȡ���ᴿ���ռ����е��������壨a��b��c��ʾ��Ӧ�����м�����Լ��������п��е��� ( )

| ���� | a | b | C | |
| A | NO2 | Ũ���� | ͭƬ | NaOH��Һ |
| B | SO2 | Ũ���� | ͭƬ | ����KMnO4��Һ |
| C | CO2 | ϡ���� | Na2CO3���� | Ũ���� |
| D | NH3 | Ũ��ˮ | ��ʯ�� | Ũ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һ�ܱ���ƿ��ע��NO2����25��ʱ��������ƽ�⣺2NO2 N2O4������ӦΪ���ȷ�Ӧ����������ƿ����100��ķ�ˮ�У������������ ��ɫ����ƽ����Է����������� �������� ѹǿ���� �ܶȡ����в������ ( )
N2O4������ӦΪ���ȷ�Ӧ����������ƿ����100��ķ�ˮ�У������������ ��ɫ����ƽ����Է����������� �������� ѹǿ���� �ܶȡ����в������ ( )
A.�ڢ� B.�ۢ� C.�ۢ� D.�٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ������������������أ�����˵����ȷ����
A�������ƿ��Ա�����ú�ͻ�ƾ��У���ֹ�ڿ����б���
B��ʯ�͵��ѻ���ú�ĸ������ڻ�ѧ�仯
C���������������Ǻ�������������ȫ�����ͷŵ��������
D��������ϩ��Ʒ����ɰ�ɫ��Ⱦ���ɲ��÷��շ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ϳɰ������ķ���ʹ��ҵ���˹��̵���Ϊ��ʵ��
(1)��֪N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H=-92��2kJ��mol-1����һ�������·�Ӧʱ�������ɱ�״����33.6LNH3ʱ���ų�������Ϊ ��
H=-92��2kJ��mol-1����һ�������·�Ӧʱ�������ɱ�״����33.6LNH3ʱ���ų�������Ϊ ��
(2)�ϳɰ������ϵ��ƽ��״̬ʱNH3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ����ͼ��֪��
 ���¶�T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1 K2 (�>����<��)�����ں��¡���ѹ�����£���ƽ����ϵ��ͨ�뺤����ƽ�� �ƶ���(����������ҡ�����)��
���¶�T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1 K2 (�>����<��)�����ں��¡���ѹ�����£���ƽ����ϵ��ͨ�뺤����ƽ�� �ƶ���(����������ҡ�����)��
��T2�¶�ʱ����1L���ܱ������м���2.1mol N2��l.5molH2����10min�ﵽƽ�⣬��v(H2)= ���ﵽƽ�����������������ͨ��N2��H2��NH3��0.4mol����ƽ�� �ƶ�(����������ҡ�����)��
(3)��ҵ����CO2��NH3��Ӧ�������أ�CO2(g)+2NH3(g) H2O(1)+CO(NH2)2(1) ��H��
H2O(1)+CO(NH2)2(1) ��H��
��һ��ѹǿ�²���������ݣ�
����÷�Ӧ��H 0����������a d��b f(��ѡ�>��������=����<��)��
�ڴ����غϳ����ڳ������������Ժ���һ������CO2��NH3��Ӧ��δ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и�ʽ�У�������ȷ�ĵ��뷽��ʽ����
A��HCO3- + H2O  H2CO3 + OH- B��HCO3- ��OH- === H2O + CO32-
H2CO3 + OH- B��HCO3- ��OH- === H2O + CO32-
C��NH3 + H+ === NH4+ D��NH3��H2O  NH4+ + OH-
NH4+ + OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ij�¶������£������й�һ�����ʵ���Ũ�ȵİ�ˮ˵����ȷ����
A����ˮ�ٽ���ˮ�ĵ���
B.  �Ǹ�����
�Ǹ�����
C��NH3��H2O����ﵽƽ��ı�־����Һ�ʵ�����
D��c(NH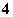 )��c(H��)��c(NH3��H2O)��c(OH��)
)��c(H��)��c(NH3��H2O)��c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��SO2ͨ�� ��Һ��������δ���г������ɣ�����ͨ����һ���壬���������ɣ�����������Ϊ�� ��
��Һ��������δ���г������ɣ�����ͨ����һ���壬���������ɣ�����������Ϊ�� ��
A��NO2 B��NH3 C�� D��CO2
D��CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ֻ��һ���Լ����ܽ����͡�������Һ�����Ȼ�̼����ϩ����������ɫҺ��ֿ����� (��������)
A. FeCl3��Һ B. NaOH��Һ C. ��ˮ D. þ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com