
| A. | 明矾净水:Al3++3H2O?Al(OH)3(胶体)+3H+ | |
| B. | 测0.1mol/L氨水的pH为11:NH3•H2O?NH4++OH- | |
| C. | 水垢中的CaSO4用Na2CO3溶液处理:Ca2++CO32-=CaCO3↓ | |
| D. | NaOH溶液的试剂瓶不能用玻璃塞:SiO2+2OH-=SiO32-+H2O |
分析 A.铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有较大的吸附面积,能够净水;
B.氨水为弱碱,一水合氨在溶液中存在电离平衡;
C.硫酸钙不能拆开,需要保留化学式;
D.二氧化硅与氢氧化钠溶液反应生成硅酸钠和水.
解答 解:A.明矾电离出的铝离子能够发生水解生成氢氧化铝胶体,发生反应为:Al3++3H2O?Al(OH)3(胶体)+3H+,氢氧化铝胶体具有吸附性,能够净水,故A正确;
B.测0.1mol/L氨水的pH为11,电离的离子方程式为:NH3•H2O?NH4++OH-,故B正确;
C.水垢中的CaSO4用Na2CO3溶液处理,正确的离子方程式为:CaSO4+CO32-=CaCO3+SO42-,故C错误;
D.氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是发生反应:SiO2+2OH-=SiO32-+H2O,生成的硅酸钠具有粘性,将玻璃塞与试剂瓶黏在一起,故D正确;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,题目难度不大题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


科目:高中化学 来源: 题型:实验题
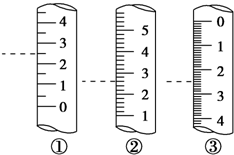 托盘天平、容量瓶、滴定管、量筒是中学化学常见的计量仪器,熟知这些仪器的使用是定量研究化学的基础.
托盘天平、容量瓶、滴定管、量筒是中学化学常见的计量仪器,熟知这些仪器的使用是定量研究化学的基础.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
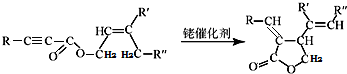
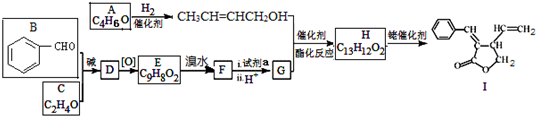
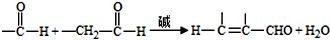
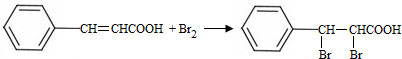 ;试剂a 是NaOH、醇溶液.
;试剂a 是NaOH、醇溶液.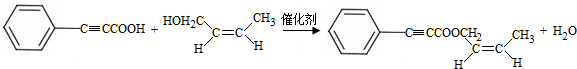 .
.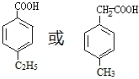 (写出一种即可).
(写出一种即可). 和CH3CHO为原料合成
和CH3CHO为原料合成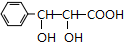 的合成路线流程图:
的合成路线流程图: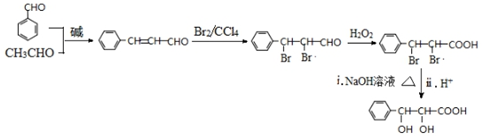 .(其它试剂任选,合成路线常用的表示方式为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)
.(其它试剂任选,合成路线常用的表示方式为:A$→_{反应条件}^{反应试剂}$B…$→_{反应条件}^{反应试剂}$目标产物)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8g18O2分子与1.8g18O3分子中含有的中子数不同 | |
| B. | 7.8gNa2S和7.8g Na2O2中含有的阴离子数目均为0.1NA | |
| C. | 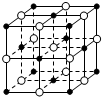 23.4 g NaCl晶体中含有0.1NA个如图所示的结构单元 | |
| D. | 含16 g氧原子的二氧化硅晶体中含有的δ键数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应物 | a+b | c+d | a+d | a+c | b+d |
| 现象 | ↓ | ↓↑ | ↓ | ↓ | ↑ |
| A. | AlCl3、HCl、AgNO3、Na2CO3 | B. | AgNO3、HCl、Na2CO3、AlCl3 | ||
| C. | Na2CO3、AlCl3、HCl、AgNO3 | D. | AgNO3、HCl、AlCl3、Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱性溶液中Na+、Cu2+、HCO${\;}_{3}^{-}$、NO${\;}_{3}^{-}$ | |
| B. | 中性溶液中Na+、Fe3+、OH-、SO${\;}_{4}^{2-}$ | |
| C. | 碱性溶液中Na+、K+、SO${\;}_{4}^{2-}$、CO${\;}_{3}^{2-}$ | |
| D. | 酸性溶液中Na+、K+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上利用氨气制硝酸属于人工固氮 | |
| B. | 明矾能够消毒杀菌是利用了胶体的吸附性 | |
| C. | 常温下,运输浓H2SO4、浓HNO3时可用铝制或铁制槽车 | |
| D. | 硅可用于制造光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 $\stackrel{③}{→}$C2H5Br,则反应①、②、③的反应类型分别为( )
$\stackrel{③}{→}$C2H5Br,则反应①、②、③的反应类型分别为( )| A. | 取代反应、加成反应、取代反应 | B. | 取代反应、取代反应、加成反应 | ||
| C. | 氧化反应、加成反应、加成反应 | D. | 氧化反应、加成反应、取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
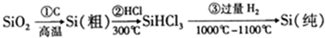 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 步骤①的化学方程式为:SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| B. | 步骤①②③中每生成或反应1mol Si,转移2mol电子 | |
| C. | 二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应 | |
| D. | SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点67.6℃),通过蒸馏(或分馏)可提纯SiHCl3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com