
分析 (1)1g甲醇液体燃烧生成CO2和液态水时放热22.0kJ,则1mol甲醇液体燃烧生成CO2和液态水时放热为22.0kJ×32=704.4kJ;
(2)每生成23g NO2需要吸收16.0kJ热量,则生成1molNO2需要吸收热量为16.0kJ×$\frac{46}{23}$=64.0kJ,结合物质的状态、焓变书写热化学方程式.
解答 解:(1)1g甲醇液体燃烧生成CO2和液态水时放热22.0kJ,则1mol甲醇液体燃烧生成CO2和液态水时放热为22.0kJ×32=704.4kJ,则表示甲醇燃烧热的热化学方程式为CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-704.0kJ/mol,
故答案为:CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-704.0kJ/mol;
(2)每生成23g NO2需要吸收16.0kJ热量,则生成1molNO2需要吸收热量为16.0kJ×$\frac{46}{23}$=64.0kJ,则热化学方程式为N2(g)+2O2(g)=2NO2(g)△H=+64.0kJ/mol,
故答案为:N2(g)+2O2(g)=2NO2(g)△H=+64.0kJ/mol.
点评 本题考查热化学方程式的书写,为高频考点,把握物质的量与热量的关系、焓变为解答的关键,侧重分析与应用能力的考查,注意燃烧热及物质的状态,题目难度不大.


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥ | B. | ②④⑤⑦ | C. | ③④⑥⑦ | D. | ②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
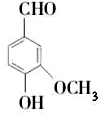 香草醛,又名香兰素,学名3-甲氧基-4-羟基苯甲醛.是食品工业和药品工业中重要的化学原料其结构简式如图所示,下列有关香草醛性质的说法中不正确的是( )
香草醛,又名香兰素,学名3-甲氧基-4-羟基苯甲醛.是食品工业和药品工业中重要的化学原料其结构简式如图所示,下列有关香草醛性质的说法中不正确的是( )| A. | 香草醛可以发生银镜反应 | |
| B. | 香草醛遇FeCl3溶液可以变紫色 | |
| C. | 香草醛在一定条件下可以与H2反应 | |
| D. | 香草醛既可以与NaOH溶液反应,也可以与NaHCO3溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2、H2SO4、MgCl2 | B. | CaCl2、HNO3、AgNO3 | ||
| C. | CaCl2、HNO3、NaCl | D. | BaCl2、HCl、NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 150 mL 1 mol•L-1的NaCl | B. | 75 mL 1.5mol•L-1的CaCl2 | ||
| C. | 150 mL 3 mol•L-1的KCl | D. | 75 mL 2 mol•L-1的NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 反应速率v正(X)=$\frac{m}{n}$ v逆(Y) | B. | 降低温度,c$\frac{c(Y)}{c(Z)}$的值变小 | ||
| C. | 增加Y的物质的量,X的转化率增大 | D. | 加入X,反应的△H增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化氢的摩尔质量为36.5g | |
| B. | 1mol H2SO4 的质量为98 g.mol-1 | |
| C. | 任何物质的摩尔质量都等于他的相对分子质量或相对原子质量 | |
| D. | CO2 的摩尔质量是H2 的摩尔质量的22倍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com