
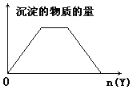
【题目】向X的溶液中,加入Y试剂,产生的沉淀示意图如图所示情形的是(注意线段的斜率)
A. 向含NaOH的NaAlO2溶液中滴加盐酸
B. 向HCl和AlCl3的混合液中滴加NaOH
C. 向NH4Cl和AlCl3的混合液中滴加NaOH
D. 向NaOH和Ca(OH)2的混合液中通入CO2
【答案】D
【解析】
A项,向含NaOH的NaAlO2溶液中滴加盐酸,随着盐酸的不断滴入,依次发生的反应为:NaOH+HCl=NaCl+H2O、NaAlO2+HCl+H2O=NaCl+Al(OH)3↓、Al(OH)3+3HCl=AlCl3+3H2O,产生的现象为:开始一段时间滴入HCl无明显现象,后开始产生沉淀,沉淀逐渐增多,沉淀达到最大时继续加入HCl,沉淀开始溶解,最终完全溶解,且产生沉淀至最大和沉淀完全溶解消耗的HCl的物质的量之比为1:3,不符合图像;
B项,向HCl和AlCl3的混合液中滴加NaOH,随着NaOH的不断滴加,依次发生的反应为:NaOH+HCl=NaCl+H2O、AlCl3+3NaOH=Al(OH)3↓+3NaCl、Al(OH)3+NaOH=NaAlO2+2H2O,产生的现象为:开始一段时间滴加NaOH无明显现象,后开始产生沉淀,沉淀逐渐增多,沉淀达到最大时继续加入NaOH,沉淀开始溶解,最终完全溶解,且产生沉淀至最大和沉淀完全溶解消耗的NaOH物质的量之比为3:1,不符合图像;
C项,向NH4Cl和AlCl3的混合液中滴加NaOH,随着NaOH的不断滴加,依次发生的反应为:AlCl3+3NaOH=Al(OH)3↓+3NaCl、NH4Cl+NaOH=NaCl+NH3·H2O、Al(OH)3+NaOH=NaAlO2+2H2O,产生的现象为:加入NaOH立即产生沉淀,沉淀逐渐增多至最大,继续滴加NaOH,一段时间沉淀不变,后沉淀开始溶解,最终完全溶解,且产生沉淀至最大和沉淀完全溶解消耗的NaOH物质的量之比为3:1,不符合图像;
D项,向NaOH和Ca(OH)2的混合液中通入CO2,随着CO2的通入,依次发生的反应为:CO2+Ca(OH)2=CaCO3↓+H2O、CO2+2NaOH=Na2CO3+H2O、CO2+Na2CO3+H2O=2NaHCO3、CO2+CaCO3+H2O=Ca(HCO3)2,产生的现象为:通入CO2立即产生沉淀,沉淀逐渐增多至最大,继续通入CO2,一段时间沉淀不变,后沉淀开始溶解,最终完全溶解,且产生沉淀至最大和沉淀完全溶解消耗的CO2物质的量之比为1:1,符合图像;
答案选D。


科目:高中化学 来源: 题型:
【题目】为了测定实验室长期存放的Na2SO3固体的纯度,准确称取M g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案I:取50.00 mL上述溶液→加入足量的盐酸酸化的BaCl2溶液→操作I→洗涤→操作Ⅱ→称量,得到沉淀的质量为m1 g
方案Ⅱ:取50.00 mL上述溶液,用a mol/L 的酸性KMnO4溶液进行滴定。
实验中所记录的数据如下表:
滴定次数 实验数据 | 1 | 2 | 3 | 4 |
待测溶液体积/mL | 50.00 | 50.00 | 50.00 | 50.00 |
滴定管初读数/mL | 0.00 | 0.20 | 0.10 | 0.15 |
滴定管末读数/mL | 20.95 | 21.20 | 20.15 | 21.20 |
(1)配制250 mL Na2SO3溶液时,必须用到的实验仪器有:烧杯、玻棒、滴管、药匙和_______________、_________________。
(2)操作I为__________________操作Ⅱ为______________
(3)方案I中如何判别加入的氯化钡已经过量______________________________
(4)在方案Ⅱ中滴定终点的判断方法是_______________________________。
(5) 在方案Ⅱ中发生的离子反应方程式为__________________________
(6)根据方案Ⅱ所提供的数据,计算Na2SO3的纯度为___________。(写成分数形式)
(7)有同学模仿方案I,提出方案Ⅲ:取50.00 mL上述溶液→加入足量的盐酸酸化的Ba(NO3)2溶液→操作I→洗涤→操作Ⅱ→称重,得到沉淀质量为m2 g 并用方案I的方法计算结果。
根据方案Ⅲ,从理论上讲,下列说法正确的是________(填序号)
a.方案I比方案Ⅲ的计算结果要低
b.方案I比方案Ⅲ的计算结果要高
c.m1=m2 ,方案I和方案Ⅲ的结果一样
d.方案Ⅲ不应根据方案I的方法计算
(8)上述实验中,由于操作错误所引起的实验误差分析正确的是__________(填序号)。
a.方案I中如果没有洗涤操作,实验结果将偏小
b.方案I中如果没有操作Ⅱ,实验结果将偏大
c.方案Ⅲ中如果没有洗涤操作,实验结果将偏小
d.方案Ⅲ中如果没有操作Ⅱ,实验结果将偏大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

完成下列填空(填元素符号或化学式):
(1)上图中元素C在周期表中的位置是___________,G和I形成的化合物不止一种,其中一种物质中各原子最外层均达到8电子稳定结构,请写出其电子式______________。
(2)请按照由大到小的顺序写出B、C、D的简单离子的离子半径大小顺序_______(用离子符号表示),上述元素中最高价氧化物对应的水化物中酸性最强的物质的化学式为___________ 。
(3)请写出D的最高价氧化物对应的水化物和F的单质反应时的离子方程式____________。
(4)元素周期表位于对角线的两种元素其性质相似称之为对角线规则。根据周期表对角线规律,金属Be单质及其化合物的性质与铝单质及其化合物的性质相似。则鉴别Be(OH)2和Mg(OH)2可选用的试剂为NaOH溶液,发生反应的化学方程式为___________。
(5)下列能说明氯元素原子得电子能力比硫元素原子得电子能力强的是___________。
① HCl的稳定性比H2S的强,② Cl2能与H2S反应生成S,③HCl的溶解度比H2S的大,④还原性:Cl-<S2-,⑤HClO4的酸性比H2SO4的强,⑥HCl的酸性比H2S的强,⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸镍((CH3COO)2Ni]是一种重要的化工原料。一种以含镍废料(含NiS、Al2O3、FeO、CaO、SiO2)为原料,制取醋酸镍的工艺流程图如下:

相关离子生成氢氧化物的pH和相关物质的溶解性如下表:

(1)粉碎含镍废料的作用__________________________________
(2)酸浸过程中,l molNiS失去6NA个电子,同时生成两种无色有毒气体。写出该反应的化学方程式:___。
(3)写出氧化步骤中加入H2O2发生反应的离子方程式:____。
(4)调节pH除铁、铝步骤中,溶液pH的调节范围是____。
(5)滤渣3主要成分的化学式是____。
(6)沉镍过程中,若c(Ni2+)= 2.0 mol.L-1,欲使100 mL该滤液中的Ni2+沉淀完全[c(Ni2+)≤10-5 mol·L-1],则需要加入Na2CO3固体的质量最少为____g(保留一位小数)。
(7)保持其他条件不变,在不同温度下对含镍废料进行酸浸,镍浸出率随时间变化如图。酸浸的最佳温度与时间分别为____℃、______min。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某铁碳合金中铁的质量分数,并探究铁与浓硫酸的反应设计了图示实验装置。

(1)在装药品开始实验前要进行的操作是_____
(2)a 克铁碳合金中加入过量浓硫酸,未点燃酒精灯前,A 无明显现象,其原因是常温下①_____;②_____。
(3)写出加热时 A 中碳与浓硫酸发生反应的化学方程式_____。
(4)B 中的现象是:_____;C 的作用是:_____。
(5)待 A 中不再逸出气体时,停止加热,拆下 E 并称重,E 增重 bg。则铁碳合金中铁的质量分数为_____(写含 a、b 的表达式)。
(6)经测定,(5)中测得结果偏小,原因可能是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化合物的元素组成的叙述,正确是
A. 蛋白质的元素组成中一定含有氮和硫
B. 脂肪的元素组成中一定含有碳和氮
C. 叶绿素的元素组成中一定含有碳和镁
D. 磷脂的元素组成中一定含有硫和磷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 由C(石墨) = C(金刚石) △H=+1.9 kJ·mol-1可知,金刚石比石墨稳定
B. 在一定条件下,等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
C. 已知2C(s) + O2(g) = 2CO(g) △H=-221 kJ·mol-1,可知C的标准燃烧热为110.5 kJ·mol-1
D. 在一密闭容器中,9.6 g的硫粉与11.2 g的铁粉混合加热,充分反应,生成硫化亚铁17.6 g,放出19.12 kJ的热量,则Fe(s) + S(s) = FeS(s) △H= - 95.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于二氧化硅的说法中错误的是 ( )
A.二氧化硅分子是由一个硅原子和两个氧原子构成的
B.在二氧化硅晶体中,每个硅原子与4个氧原子相连
C.石英、水晶、玛瑙的主要成分都是二氧化硅
D.自然界中二氧化硅主要存在于石英矿和硅酸盐中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com