
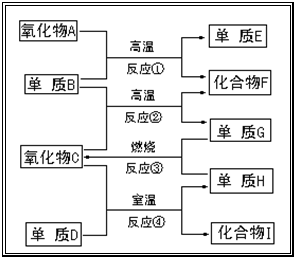
分析 单质E可作为半导体材料,应为Si,则A应为SiO2,B为C单质,F是一种具有可燃性的氧化物,应为CO,结合转化关系可知C为H2O,G为H2,H为O2,D为F2,I为HF,以此解答该题.
解答 解:单质E可作为半导体材料,应为Si,则A应为SiO2,B为C单质,F是一种具有可燃性的氧化物,应为CO,结合转化关系可知C为H2O,G为H2,H为O2,D为F2,I为HF,
(1)由以上分析可知F为CO,I为HF,故答案为:CO;HF;
(2)反应①为工业制备粗硅的反应,化学方程式为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$2CO+Si,故答案为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$2CO+Si.
点评 本题考查无机物的推断,是一道常规的框图推断题,要求学生在全面系统地掌握元素及化合物性质的基础上,善于抓住某些元素的特殊性质为解题的突破口和切入点,如本题中的半导体材料、不成盐氧化物等,题目难度不大,有利于培养学生良好的科学素养.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:O>S>Se | |
| B. | 单质的化学活动性:Cl2>F2>I2 | |
| C. | 气态氢化物的稳定性:H2O>H2S>H2Se | |
| D. | 最高价氧化物对应水化物的碱性:LiOH>NaOH>KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲基橙呈黄色的溶液中:I-、Cl-、NO${\;}_{3}^{-}$、Na+ | |
| B. | 石蕊呈蓝色的溶液中:Na+、AlO${\;}_{2}^{-}$、NO${\;}_{3}^{-}$、HCO${\;}_{3}^{-}$ | |
| C. | 含大量Al3+的溶液中:K+、Na+、NO${\;}_{3}^{-}$、ClO- | |
| D. | 含大量OH-的溶液中:CO${\;}_{3}^{2-}$、Cl-、F-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林可作食品的保鲜剂 | |
| B. | 乙烯可作水果的催熟剂 | |
| C. | 做衣服的棉和麻均与淀粉互为同分异构体 | |
| D. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
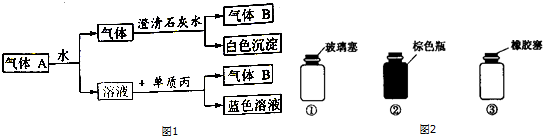
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com