
| �������� | ���� | |
| A | 100mLH2O | ��ˮ�������c��H+��•c��OH-����С |
| B | 0.01molK2O | ��Һ��$\frac{{c��{HC{O^-}}��}}{{c��{O{H^-}}��}}$���� |
| C | 50mLmol•L-1H2SO4 | ��Ӧ������c��K+��=c��SO42-�� |
| D | 0.1molKHSO4���� | ��Ӧ����������Һ��pH=7 |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� n��K2CO3��=0.1mol��̼�����ǿ�������Σ�̼�������ˮ�����Һ�ʼ��ԣ�ˮ�ⷽ��ʽΪCO32-+H2O?HCO3-+OH-��
A����ˮ̼��ص�Ũ�ȼ�С����Һ�ļ��Լ�С��
B��K2O��ˮ��Ӧ����KOH����Һ������������Ũ������
C��0.1molK2CO3�м�����Ϊ0.2mol��50mL1mol/LH2SO4�����������Ϊ0.05mol��
D��KHSO4��K2CO3��Ӧ����ʽΪ��2KHSO4+K2CO3=K2SO4+H2O+CO2�������ݷ���ʽ֪������ǡ�÷�Ӧ����K2SO4��H2O��CO2����Һ�е�����������أ�
��� �⣺n��Na2CO3��=0.05mol��̼������ǿ�������Σ�̼�������ˮ�����Һ�ʼ��ԣ�ˮ�ⷽ��ʽΪCO32-+H2O?HCO3-+OH-��
A����ˮ̼��ص�Ũ�ȼ�С����Һ�ļ��Լ�С��ˮ�ĵ���̶ȼ�С������ˮ��������������Ӻ�������Ũ�ȼ�С��������ˮ�������c��H+��•c��OH-����С����A����
B��K2O��ˮ��Ӧ����KOH����Һ������������Ũ������������K2CO3��ˮ�⣬������Һ��$\frac{{c��{HC{O^-}}��}}{{c��{O{H^-}}��}}$��С����B����
C��0.1molK2CO3�м�����Ϊ0.2mol��50mL1mol/LH2SO4�����������Ϊ0.05mol��������Һ�У�K+��=4c��SO42-������C����
D��KHSO4��K2CO3��Ӧ����ʽΪ��2KHSO4+K2CO3=K2SO4+H2O+CO2�������ݷ���ʽ֪������ǡ�÷�Ӧ����K2SO4��H2O��CO2����Һ�е�����������أ���Һ�����ԣ���ҺpH=7����D��ȷ��
��ѡD��
���� ���⿼��������ˮ��ԭ��������Ũ�ȴ�С�Ƚϣ����ؿ���ѧ�������жϼ�������������ȷ����֮��ķ�Ӧ����Һ�����ʳɷּ��������ǽⱾ��ؼ���ע�����غ�������غ����ȷ���ã���Ŀ�ѶȲ���


 �¿α�������������ҵ�������γ�����ϵ�д�
�¿α�������������ҵ�������γ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
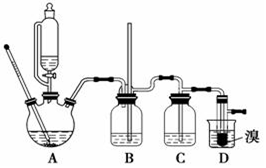 ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�CH3CH2OH��CH2=CH2$\stackrel{Br_{2}}{��}$BrCH2CH2Br����������������Ҵ��Ʊ�1��2-���������װ����ͼ��ʾ��
ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�CH3CH2OH��CH2=CH2$\stackrel{Br_{2}}{��}$BrCH2CH2Br����������������Ҵ��Ʊ�1��2-���������װ����ͼ��ʾ��| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | -130 | 9 | -116 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2mol/L | B�� | 1 mol/L | C�� | 0.01 mol/L | D�� | 0.22 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ۼ���ϡ�����У�2Fe+6H+�T2Fe3++3H2�� | |
| B�� | �ƺ���ˮ��Ӧ Na+2H2O=Na++2OH-+H2�� | |
| C�� | ����ͭ��Ba��OH��2��Һ��Ӧ��Cu2++2OH-=Cu��OH��2�� | |
| D�� | ʵ�����ô���ʯ��ϡ������ȡCO2��2H++CaCO3�TCa2++CO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ��ʾ��װ�ã�C��D��E��F��X��Y�����Ե缫������Դ��ͨ�������е����̪��Һ����F�������Ժ�ɫ��������˵����ȷ���ǣ�������
��ͼ��ʾ��װ�ã�C��D��E��F��X��Y�����Ե缫������Դ��ͨ�������е����̪��Һ����F�������Ժ�ɫ��������˵����ȷ���ǣ�������| A�� | ��ԴB���Ǹ��� | |
| B�� | �ס���װ�õ�C��D��E��F�缫���е������ɣ������ʵ���֮��Ϊ1��2��2��2�� | |
| C�� | װ�ö���Y���������ɫ���˵��������������������� | |
| D�� | ���ñ�װ�ø�ͭ������HӦ����Ag�����Һ��AgNO3��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 58.5g NaCl����1Lˮ�����1mol/L NaCl��Һ | |
| B�� | �ڱ�״���£�44.8LHCl��������ˮ���1L��Һ��������Һ�����ʵ����ʵ���Ũ��Ϊ2mol/L | |
| C�� | �ڱ�״���£�22.4L��������ˮ���1L��Һ����������Һ��ȡ��10mL�������ʵ���Ũ��Ϊ1mol/L | |
| D�� | 1mol/L��CaCl2��Һ1L��ȡ��100mL����0.2molCl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼΪij��ѧ��Ӧ��������ʱ��Ĺ�ϵʾ��ͼ����t1ʱ�������¶Ȼ�������ѹǿ�����ʵı仯�����ϵ�ʾ��ͼ�ķ�Ӧ�ǣ�������
��ͼΪij��ѧ��Ӧ��������ʱ��Ĺ�ϵʾ��ͼ����t1ʱ�������¶Ȼ�������ѹǿ�����ʵı仯�����ϵ�ʾ��ͼ�ķ�Ӧ�ǣ�������| A�� | 2SO2��g��+O2��g��?2SO3��g�� H��0 | B�� | 4NH3��g��+5O2��g��?4NO��g��+6H2O��g�� H��0 m | ||
| C�� | H2��g��+I2��g��?2HI��g�� H��0 | D�� | N2��g��+3H2��g��?2 NH3��g�� H��0 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com