
下列实验装置图合理的是 

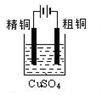

① ② ③ ④
| A.装置①可用于证明溴乙烷、NaOH、乙醇溶液共热生成乙烯 |
| B.装置②能构成锌铜原电池 |
| C.装置③可用于粗铜的电解精炼 |
| D.装置④可用于在实验室测定中和反应的反应热 |
科目:高中化学 来源: 题型:单选题
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸
氧腐蚀相同。下列分析正确的是
| A.含有 1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
| B.脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e-=4OH- |
| D.脱氧过程中铁作原电池正极,电极反应为:Fe-3e-=Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2(s)+Pb(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(I),根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb+SO42--2e-=PbSO4↓ |
| C.PbO2得电子,被氧化 |
| D.电池放电时,溶液酸性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
图中,两电极上发生的电极反应分别为:a极:Ag++e-=Ag b极:Fe-2e-=Fe2+;下列说法不正确的是( )
| A.a、b可能是同种电极材料 |
| B.该装置一定是电解池 |
| C.装置中电解质溶液一定含有Ag+ |
| D.装置中发生的反应方程式一定是Fe+2Ag+==Fe2++2Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用惰性电极实现下列电解实验,其说法正确的是
| A.电解稀硫酸溶液,实质上是电解水,故溶液的pH不变 |
| B.电解稀氢氧化钠溶液,阳极消耗OH-,故溶液的pH减小 |
| C.电解硫酸钠溶液,阴极和阳极析出产物的物质的量之比为2:1 |
| D.电解氯化铜溶液,通电一段时间后,向溶液中加入适量的CuO或CuCO3均可使电解液恢复到起始状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用压强传感器探究生铁在pH=2和pH=4醋酸溶液中发生腐蚀的装置及得到的图像如下: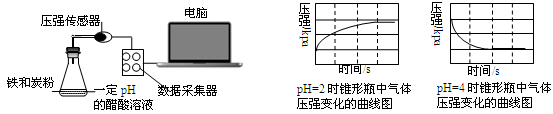
分析图像,以下结论错误的是
| A.溶液pH≤2时,生铁发生析氢腐蚀 | B.在酸性溶液中生铁可能发生吸氧腐蚀 |
| C.析氢腐蚀和吸氧腐蚀的速率一样快 | D.两溶液中负极反应均为:Fe – 2e→Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列事实解释准确的是
| A.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。脱氧过程中铁作原电池正极,电极反应为:Fe-2 e-=Fe2+ |
| B.酸性氢氧燃料电池的正极电极反应为:2H2O+O2+4e-=4OH- |
| C.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,该反应的△S>0,说明反应△H>0 |
| D.铅蓄电池的正极反应为:PbO2+4H++2 e-=Pb2++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某同学设计的铜锌原电池如右图所示,则下列说法正确的是
| A.因为锌与硫酸锌,铜与硫酸铜不反应,所以该装置无法工作 |
| B.电池反应为:Zn2++Cu=Zn +Cu2+ |
| C.盐桥中的Cl-移向ZnSO4溶液 |
| D.在外电路中,电流从负极流向正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验现象预测正确的是(双选) ( )。
| A.实验Ⅰ:电流表A指针偏转,碳棒上有红色固体析出 |
| B.实验Ⅱ:电流表A指针偏转,铁极上有无色气体产生 |
| C.实验Ⅲ:碳棒上有无色气体产生,铁极上有黄绿色气体产生 |
| D.实验Ⅳ:粗铜溶解,精铜上有红色固体析出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com