
【题目】(1)实验室用金属铜和稀硝酸制取NO的离子方程式为______________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图甲所示。

①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填序号)。
A.铁 B.铝 C.铂 D.玻璃
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是__________(填化学方程式)。
(3)为证明铜丝与稀硝酸反应生成的确实是NO,某学生另设计了一套如图乙所示的装置制取NO。反应开始后,可以在U形管右端观察到无色的NO气体。
①长玻璃管的作用是______________________________________________________。
②让反应停止的操作方法及原因是__________________________________________。
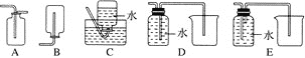
(4)以下收集NO气体的装置,合理的是________(填序号)。
(5)将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:
①NO的体积为________ L,NO2的体积为________ L。
②待产生的气体全部释放后,向溶液中加入VmLamol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为________ mol·L-1。
【答案】3Cu+8H++2NO![]() =3Cu2++4H2O+2NO↑ CD 2NO+O2=2NO2 接收被气体压出U形管的液体,防止稀硝酸溢出 关闭U形管右端导气管上的活塞;反应产生的气体将U形管右端管内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止 CD 5.8 5.4
=3Cu2++4H2O+2NO↑ CD 2NO+O2=2NO2 接收被气体压出U形管的液体,防止稀硝酸溢出 关闭U形管右端导气管上的活塞;反应产生的气体将U形管右端管内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止 CD 5.8 5.4 ![]()
【解析】
(1)金属铜和稀硝酸反应生成硝酸铜和NO气体;
(2)①由题意可知,这种成分不能与稀硝酸反应,而Fe、Al与硝酸反应,所以AB不行;
②二氧化氮是红棕色的气体,一氧化氮很容易和空气中的氧气化合,生成红棕色的二氧化氮气体;
(3)①为了证明产生的气体是NO,则该实验装置要防止产生的气体与空气接触,长玻璃管可以接收被气体压出U形管的液体,防止稀硝酸溢出;
②关闭U形管右端导气管上的活塞,反应产生的气体使稀硝酸液面下降,从而使铜丝与稀硝酸分开,反应停止;
(4)NO能与空气中的氧气反应,故不能用排空气法收集NO,只能用排水法收集;
(5)根据守恒的原理计算NO、NO2的体积,以及硝酸溶液的浓度。
(1)金属铜和稀硝酸反应生成硝酸铜和NO气体,反应的化学方程式:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,离子方程式为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O。
(2)①由题意可知,这种成分不能与稀硝酸反应,而Fe、Al与硝酸反应,所以AB不行,故答案为:CD。
②一氧化氮很容易和空气中的氧气化合,生成红棕色的二氧化氮气体,所以,制取一氧化氮的装置打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,发生2NO+O2═2NO2,
故答案为:2NO+O2═2NO2。
(3)①为了证明产生的气体是NO,则该实验装置要防止产生的气体与空气接触,长玻璃管可以接收被气体压出U形管的液体,防止稀硝酸溢出,故答案为:接收被气体压出U形管的液体,防止稀硝酸溢出。
②关闭U形管右端导气管上的活塞,反应产生的气体使稀硝酸液面下降,从而使铜丝与稀硝酸分开,反应停止,故答案为:关闭U形管右端导气管上的活塞;反应产生的气体将U形管右端管内的稀硝酸向下压,使铜丝与稀硝酸分开,反应就会停止。
(4)NO能与空气中的氧气反应,故不能用排空气法收集NO,只能用排水法收集,C和D装置符合题意,E装置是洗气装置,故答案为:CD。
(5)①设混合气中NO和NO2的物质的量分别是x和y。
则x+y=11.2L÷22.4L/mol=0.5mol ①
金属铜的物质的量是32.64g÷64g/mol=0.51mol
则根据电子的得失守恒可知n(e-)=3x+y=2n(Cu2+)=0.51mol×2 ②
由①、②解得x=0.26mol、y=0.24mol
所以NO和NO2的体积分别是0.26mol×22.4L/mol=5.8L,0.24mol×22.4L/mol=5.4L。
故答案为:5.8,5.4。
②溶液中的Cu2+全部转化成沉淀后,溶液中的溶质恰好是硝酸钠,
则根据原子守恒可知,硝酸钠的物质的量是0.001Vamol
所以原硝酸溶液的浓度为![]() =
=![]()
故答案为: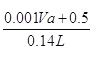 。
。


科目:高中化学 来源: 题型:
【题目】在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸;当X无论是强酸还是强碱时,都有如下的转化关系:
![]()
当X是强酸时A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。
请回答:
(1)A是________,Y是________,Z是________。
(2)当X是强酸时,E是________,写出B生成C的化学方程式:________________________
(3)当X是强碱时,E是________,写出B生成C的化学方程式:________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据物质结构有关性质和特点,回答下列问题:
(1)Ti基态原子核外电子排布式为 _____基态铝原子核外电子云形状有_________(填名称)。
(2)丙烯腈(CH2=CH-CN)分子中α键和![]() 键的个数比为_____,分子中碳原子轨道的杂化类型是___
键的个数比为_____,分子中碳原子轨道的杂化类型是___
(3)写出与NH4+互为等电子体的一种分子和一种离子的化学式______、_______。
(4)钛存在两种同素异构体,![]() 采纳六方最密堆积,
采纳六方最密堆积,![]() 采纳体心立方堆积,鉴别两种钛晶体可以用_____法,由
采纳体心立方堆积,鉴别两种钛晶体可以用_____法,由![]() 转变为
转变为![]() 晶体体积_____(填“膨胀”或“收缩”)。
晶体体积_____(填“膨胀”或“收缩”)。
(5)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用____________形象化描述。
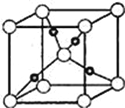
(6)Cu与O元素形成的某种化合物的晶胞结构如图所示,晶胞中氧原子的配位数为____,若阿伏伽德罗常数为NA,晶胞的边长为a pm,该晶体的密度为__gcm﹣3.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为原子序数依次增大的短周期元素A~F的第一到第五电离能数据,表中的金属元素是
电离能I(ev) | A | B | C | D | E | F |
I1 | 5.2 | 7.6 | 6.0 | 11.3 | 13.6 | 14.5 |
I2 | 49.3 | 15.0 | 18.8 | 24.4 | 35.1 | 29.6 |
I3 | 71.6 | 80.1 | 28.4 | 47.9 | 54.9 | 47.4 |
I4 | 98.9 | 109.2 | 112.0 | 64.5 | 77.4 | 77.5 |
I5 | 138.3 | 141.3 | 153.7 | 392.1 | 113.9 | 97.9 |
A.A B CB.B C DC.C D ED.D E F
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y均为有刺激性气味的气体,且几种物质间有以下转化关系,部分产物未标出。

回答下列问题:
(1)写出下列各物质的化学式:X____、Y_____、A_____、B_____、C____。
(2)反应①的的化学方程式为_____,反应②的离子方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于NaHCO3性质的有关叙述正确的是( )
A. 只能与强酸反应,不能与强碱反应
B. 医疗上可用于治疗胃酸过多
C. 与足量的酸反应时放出的CO2比等质量的Na2CO3要少
D. 同温度时,NaHCO3的溶解度>Na2CO3的溶解度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2Fe3++SO32-+H2O![]() 2Fe2++SO42-+2H+。如图所示是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,G是灵敏电流计,其指针总是偏向电源负极。A杯中为FeCl3溶液;B杯中为Na2SO3溶液。以下关于该装置的说法错误的是
2Fe2++SO42-+2H+。如图所示是一套电化学实验装置,图中C、D均为铂电极,U为盐桥,G是灵敏电流计,其指针总是偏向电源负极。A杯中为FeCl3溶液;B杯中为Na2SO3溶液。以下关于该装置的说法错误的是

A.G的指针指向B极
B.U中阳离子向A极移动
C.一段时间后,化学反应达到平衡状态,导线中无电流通过
D.一段时间后,B中溶液pH增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com