
| A. | 4mL | B. | 10.8mL | C. | 1.2mL或4mL | D. | 8mL或10.8mL |
分析 假定全部为二氧化氮,剩余气体体积为$\frac{1}{3}$×12mL=4mL,大于实际剩余2mL气体,则说明剩余气体为NO或氧气.
若剩余气体为氧气,根据4NO2+O2+2H2O=4HNO3,求NO2的体积,总体积减去NO2的体积可得混合气体中氧气的体积;
若剩余气体为NO,先根据3NO2+H2O=2HNO3+2NO求出过量的NO2,然后根据4NO2+O2+2H2O=4HNO3求出O2的体积.
解答 解:假定全部为二氧化氮,剩余气体体积为$\frac{1}{3}$×12mL=4mL,大于实际剩余2mL气体,则说明剩余气体为NO或氧气.
若剩余气体为氧气,则参加反应的气体为12mL-2mL=10mL,根据4NO2+O2+2H2O=4HNO3,可知参加此反应的NO2的体积为10mL×$\frac{4}{5}$=8mL,参加反应的O2的体积为10mL-8mL=2mL,原混合气体中O2的体积为2mL+2mL=4mL;
若剩余气体为NO气体,根据3NO2+H2O=2HNO3+NO,可知过量的NO2为3×2mL=6mL,反应4NO2+O2+2H2O=4HNO3消耗的气体总体积为12mL-6mL=6mL,则反应消耗的氧气为6mL×$\frac{1}{5}$=1.2mL,
故选:C.
点评 本题考查混合物有关计算、氮氧化物的性质等,关键是分析判断剩余气体的成分,注意对总反应方程式的运用.


科目:高中化学 来源: 题型:解答题
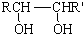 $→_{△}^{HIO_{4}}$ RCHO+R′CHO
$→_{△}^{HIO_{4}}$ RCHO+R′CHO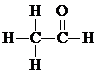 .
.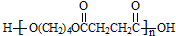 .
.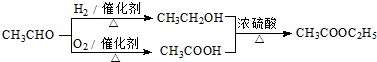
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若a<b,则c<$\frac{1}{2}$(a+b) | B. | 若a<b,则c>$\frac{1}{2}$(a+b) | C. | 若a>b,则c=$\frac{1}{2}$(a+b) | D. | 若a=b,则c=$\frac{1}{2}$(a+b) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
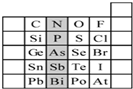 元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.请用元素符号或化学式填空:
元素在周期表中的位置,反映了元素的原子结构和元素的性质.下图是元素周期表的一部分.请用元素符号或化学式填空:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属性A>B>D | |
| B. | B和C形成的化合物中可能有共价键 | |
| C. | 原子序数D>C>A>B | |
| D. | 四种元素中,最高价氧化物对应的水化物酸性最强的是B |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素性质 | 元素编号 | |||||||
| A | B | C | D | E | F | G | H | |
| 原子半径(nm) | 0.102 | 0.117 | 0.074 | 0.110 | 0.071 | 0.075 | 0.077 | 0.099 |
| 最高化合价 | +6 | +4 | +5 | +5 | +4 | +7 | ||
| 最低化合价 | -2 | -4 | -2 | -3 | -1 | -3 | -4 | -1 |
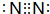 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑥ | B. | ②③⑤ | C. | ①②④ | D. | ①③⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com