
| A. | ①③⑤ | B. | ①⑥⑦ | C. | ②④⑦ | D. | ②③④⑤ |
分析 ①水蒸气的能量比液态水高;②中和反应是放热反应;③浓酸的稀释是放热的;④氢氧化钠固体俗称烧碱,溶于水放热;⑤所有的燃烧均是放热;⑥C与高温水蒸气生成水煤气是吸热;⑦铵盐与碱反应是吸热反应.
解答 解:①水蒸气的能量比液态水高,故液态水变成水蒸气需要吸热;
②中和反应是放热反应;
③浓酸的稀释是放热的,即浓硫酸稀释放热;
④氢氧化钠固体俗称烧碱,溶于水放热;
⑤所有的燃烧均是放热,故H2在Cl2中燃烧也是放热反应;
⑥C与高温水蒸气生成水煤气是吸热;
⑦铵盐与碱反应是吸热反应,故NH4Cl晶体与Ba(OH )2•8H2O混合搅拌吸热,故属于放热的是②③④⑤,故选D.
点评 本题考查化学反应中能量变化,题目难度不大,掌握常见的放热反应和吸热反应是解题的关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
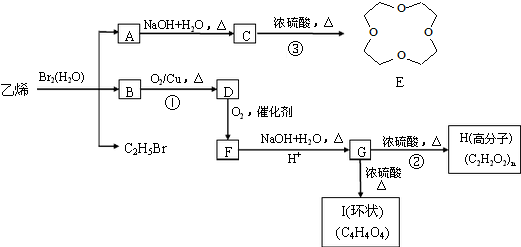
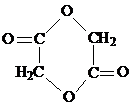 .
.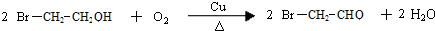 .写出反应 ②的化学方程式
.写出反应 ②的化学方程式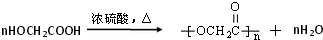 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验蔗糖水解产物中的葡萄糖 | 取1mL 20%蔗糖溶液,加入少量稀硫酸,水浴加热后取少量溶液于另一试管中,加入几滴新制Cu(OH)2,加热 |
| B | 除去乙烷中混有的少量乙烯 | 将混合气体通入足量酸性KMnO4溶液中 |
| C | 检验葡萄糖中含有醛基 | 向3mL 2%氨水溶液中加入几滴2%的硝酸银溶液,再加入1mL10%的葡萄糖溶液温水浴加热几分钟 |
| D | 验证蛋白质的盐析 | 向豆浆、鸡蛋清溶液中均滴加饱和硫酸铵溶液,振荡至出现沉淀,再向沉淀物中加入蒸馏水,不断振荡 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯和乙苯 | B. | 乙烯和丁烯 | C. | 甲烷和丙烯 | D. | 乙炔和丁炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | v正(NH3)=3v逆(H2) | |
| B. | 1个N≡N键断裂的同时有6个N-H键断裂 | |
| C. | 反应体系压强不再变化 | |
| D. | 混合气体质量不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由长、短周期元素共同组成的元素族称为主族 (除零族外) | |
| B. | 同一元素不可能既表现金属性,又表现非金属性 | |
| C. | 短周期元素原子形成简单离子后,最外层电子都达到8电子稳定结构 | |
| D. | 互为同位素的不同核素,物理性质和化学性质都不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中滴加盐酸酸化的BaCl2溶液出现被色沉淀,则溶液中不一定存在SO${\;}_{4}^{2-}$ | |
| B. | 形成酸雨的氧化物主要是SO2和氮的氧化物,CO2是造成温室效应的主要气体 | |
| C. | 氯气泄漏自救方法是用湿毛巾或蘸有纯碱水的毛巾捂住口鼻并向地势低的地方撤离 | |
| D. | 大气中的N2可转化为NO,NO可转化为NO2、硝酸等,含硫物质在自然界中可转化为SO2等含硫化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com