
【题目】单质A、B、C在一定条件下,可以按下面的流程进行反应.已知单质A、B常温下分别为无色气体和黄绿色气体,单质C是常见的金属,D的水溶液常温下能与单质C反应生成F和单质A. 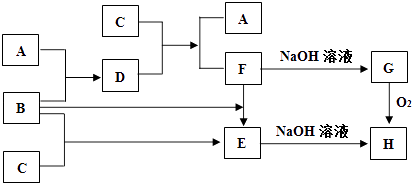
请完成下列填空:
(1)写出单质B的化学式 , D物质的电子式 .
(2)写出E→H的化学方程式 .
(3)写出D+C→F+A的离子方程式 .
【答案】
(1)Cl2;
(2)FeCl3+3NaOH═Fe(OH)3↓+3NaCl
(3)Fe+2H+=Fe2++H2↑
【解析】解:B为黄绿色气体单质,所以B为氯气,A为无色气体,A与氯气反应生成D,D与金属C反应又得A,所以A为氢气,D为氯化氢,F为含C金属元素的盐,G为C金属元素的碱,B、C反应生成E,E与碱反应生成H,G氧化得H,说明C中含有的金属元素为可变价元素,C是常见的金属,据此可推知C为铁,F为氯化亚铁,G为氢氧化亚铁,E为氯化铁,H为氢氧化铁,(1)根据上面的分析可知,单质B的化学式为Cl2 , D为氯化氢,D物质的电子式 ![]() ,所以答案是:Cl2;
,所以答案是:Cl2; ![]() ;(2)E→H的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl,所以答案是:FeCl3+3NaOH═Fe(OH)3↓+3NaCl; (3)D+C→F+A的离子方程式为Fe+2H+=Fe2++H2↑,所以答案是:Fe+2H+=Fe2++H2↑.
;(2)E→H的化学方程式为FeCl3+3NaOH═Fe(OH)3↓+3NaCl,所以答案是:FeCl3+3NaOH═Fe(OH)3↓+3NaCl; (3)D+C→F+A的离子方程式为Fe+2H+=Fe2++H2↑,所以答案是:Fe+2H+=Fe2++H2↑.


科目:高中化学 来源: 题型:
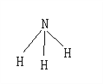
【题目】已知断裂1molH-H要吸收的能量为436kJ,形成1molH-N放出391kJ的能量,氨气的结构如图,根据化学方程式N2+3H2 ![]() 2NH3,1molN2与3molH2反应时放热92kJ,则断裂1molN≡N所需要的能量为 ( )
2NH3,1molN2与3molH2反应时放热92kJ,则断裂1molN≡N所需要的能量为 ( )
A. 431kJ B. 698kJ C. 946kJ D. 394kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在生产、生活中有着广泛的应用。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体,同时得到浅绿色酸性溶液。为此,他们设计了如下装置验证所产生的气体(夹持装置省略)并进行有关实验。

(1)①若装置A中的试管不加热,则没有明显现象,原因是____________。
②证明有SO2 生成的现象是_____;为了证明气体中含有氢气,装置B和C中加入的试剂分别为X、CuSO4,请写出装置B处反应的化学方程式________________。
(2)取装置A试管中的溶液6mL,加入适量氯水恰好反应,再加入过量的KI溶液后,分别取2mL此溶液于3支小试管中进行如下实验:
①第一支试管中加入1mLCCl4,充分振荡、静置,CCl4层呈紫色;
②第二支试管中加入1滴K3[Fe(CN)6] 溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是________________(填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有____(填离子符号),由此可以证明该离子与I-发生的氧化还原反应为_______。
(3)向盛有H202溶液的试管中加入几滴装置A试管中的溶液,溶液变成棕黄色,发生反应的离子方程式为_________________;一段时间后,溶液中有气泡出现并放热,随后有红褐色沉淀生成。产生气泡的原因是________________;生成沉淀的原因是_______________ (用平衡移动原理解释)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述中正确的是
A.正极和负极必须是两种不同的金属
B.电子流入的一极为正极
C.原电池工作时,正极和负极上发生的都是氧化还原反应
D.原电池工作时,实现了将电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从下列事实所列出的相应结论正确的是( )
实验事实 | 结论 | |
① | 铜生的锈是绿色的称为铜绿 | 铜绿是致密的氧化膜 |
② | 浓硫酸可除去烧瓶内残留的MnO2 , 稀硝酸可除去试管内壁的银镜,用磨口玻璃瓶保存NaOH溶液 | 都发生了氧化还原反应 |
③ | 少量CO2通入Na[Al(OH)4]溶液产生白色沉淀和Na2CO3 | 酸性:HCO3﹣>Al(OH)3 |
④ | 某溶液加入稀盐酸产生能使澄清石灰水变浑浊的无色无味气体,该溶液滴加CaCl2溶液,有白色沉淀现象 | 确定该溶液存在CO |
⑤ | 某无色溶液中加入浓氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH |
A.②③⑤
B.①②③
C.③④⑤
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏
B.萃取、蒸馏、分液
C.分液、蒸馏、萃取
D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应速率的说法正确的是:
A. 用铁片和稀硫酸反应制氢气时,改用98%的硫酸可以加快反应速率
B. 100 mL 2 molL﹣1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C. 反应C(s)+H2O(g) ![]() CO(g)+H2(g)在一可变容积的密闭容器中进行,增加C的量 , 其反应速率增大
CO(g)+H2(g)在一可变容积的密闭容器中进行,增加C的量 , 其反应速率增大
D. 汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率变慢:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com