
���� ��1���ɷ���ʽ��֪����Ӧǰ�����������������仯���ݴ˼��������������
��2����״���£�����Ħ������M=Vm���ѣ��ݴ˼�������X2��Ħ�����������ݷ���ʽ��������ʵ���X2Y4���ټ���X2Y4����Է�����������������Y�����ԭ��������ȷ��YԪ�����ƣ�
��3������X2��g����2H2O���м��㣮
��� �⣺��1���ɷ���ʽ��֪����Ӧǰ�����������������仯��X2�������Ĺ�ϵʽΪ1��1����V��O2��=V��X2��=22.4L��
�ʴ�Ϊ��22.4��
��2����״���£�����Ħ������M=Vm���ѣ�����X2��Ħ������=22.4L/mol��1.25g/L=28g/mol��
22.4L X2�����ʵ���=$\frac{22.4L}{22.4L/mol}$=1mol��n��X2Y4��=n��X2��=1mol����Mr��X2Y4��=$\frac{32}{1}$=32����Y�����ԭ������=$\frac{32-28}{4}$=1 ��YΪ��Ԫ�أ�
�ʴ�Ϊ��28g/mol���⣻
��3��X2��g����2H2O��l��
1 36
0.1 3.6
�ʴ�Ϊ��3.6��
���� ���⿼�黯ѧ����ʽ���йؼ��㣬�ѶȲ���ע����ݷ���ʽ������������������������������Ħ���������ܶȵĹ�ϵ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
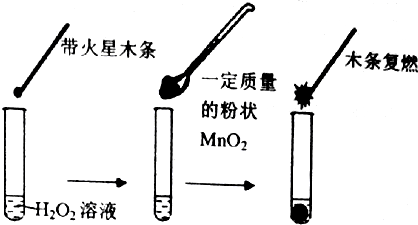
| �Թ� | �� | �� | �� |
| �μ��Լ� | 5��0.1mol•L-1FeCl3 | 5��0.1mol•L-1��CuCl2 | 5��0.3mol•L-1��NaCl |
| ����������� | �Ͽ����ϸС���� | ��������ϸС���� | �����ݲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ��Ϊͬ���칹�� ��Ϊͬ���칹�� | |
| B�� |  �� �� ��������Ϊͬϵ�� ��������Ϊͬϵ�� | |
| C�� | �ױ����������ķ�Ӧ�����ܷ�Ӧ������Ӱ�����ͬ | |
| D�� | H2��D2��Ϊͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{3a}{2}$ mol | B�� | $\frac{a}{18}$ mol | C�� | $\frac{a}{27}$ mol | D�� | $\frac{a}{96}$ mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | AlCl3 | B�� | NaOH | C�� | HCl | D�� | Na2CO3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com