
| ||
| ||
| 编号 | ① | ② | ③ | ④ | ⑤ | ||
| x值 | x=
| ||||||
| 残留固体及 物质的量 | Si
|
| ||
| ||
| ||
| 1 |
| 3 |
| 1 |
| 4 |
| 1 |
| 3 |
| 1 |
| 4 |
| 1 |
| 3 |
| 1 |
| 4 |
| ||
| ||
| ||
| 1 |
| 3 |
| 1 |
| 3 |
| 1 |
| 4 |
| 1 |
| 4 |
| 1 |
| 3 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1-x |
| 2 |
| 1-x |
| 2 |
| 3x-1 |
| 2 |
| 1 |
| 4 |
| 1 |
| 3 |
| 1 |
| 4 |
| 编号 | ① | ② | ③ | ④ | ⑤ | ||||||||||||
| x值 | x=
| x=
|
|
| 0<x<
| ||||||||||||
| 残留固体及 物质的量 | Si
| SiC
| Si
SiO2
| Si(4x-1)mol SiC(1-3x)mol | SiC xmol C(1-4x)mol |


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
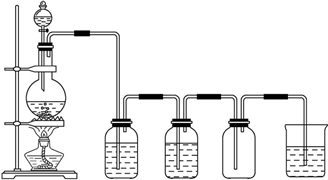
查看答案和解析>>
科目:高中化学 来源: 题型:
| CO | 2- 3 |
| SO | 2- 4 |
| A、少量H2SO4溶液 |
| B、少量HNO3溶液 |
| C、足量NaOH溶液 |
| D、足量盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、每生成1mol Na2H3IO6转移2mol电子 |
| B、碱性条件下,NaIO3的氧化性强于Na2H3IO6 |
| C、该反应中Cl2做还原剂 |
| D、氧化产物与还原产物的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2和活性炭均能使品红溶液褪色 |
| B、对碘晶体和碳酸氢铵晶体加热,晶体均会逐渐消失 |
| C、实验室配制FeCl3和SnCl2溶液时,先将固体FeCl3和SnCl2分别溶解在浓盐酸中,再加蒸馏水稀释 |
| D、SO2能使滴加酚酞的NaOH溶液和酸性KMnO4溶液的红色都褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
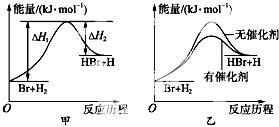
| A、正反应吸热 |
| B、加入催化剂,该化学反应的反应热不变 |
| C、加入催化剂后,该反应的能量对反应历程的示意图可用图乙表示 |
| D、加入催化剂可增大正反应速率,降低逆反应速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com