
 .
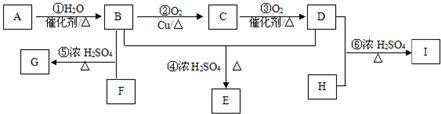
. 分析 某气态烃A与H2的相对密度为14,Mr(A)=14×2=28,其产量可以用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,C进一步发生氧化反应生成D为CH3COOH,乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3.芳香族化合物F为C、H、O化合物,1mol F与足量NaHCO3溶液反应能生成2mol CO2,则F含有2个羧基,其相对分子质量为166,2个羧基、1个C6H4的总式量为45×2+(12×6+4)=166,则F含有1个苯环、2个羧基,且环上的一氯代物有一种,则F为 ,F与足量的B发生酯化反应生成G为
,F与足量的B发生酯化反应生成G为 ,H为二元醇,其蒸气密度折算成标准状况为2.77g/L,其相对分子质量为22.4×2.77=62,去掉2个羟基剩余基团式量为62-17×2=28,故为-C2H4-,则H为HOCH2CH2OH,H与足量D反应生成I为
,H为二元醇,其蒸气密度折算成标准状况为2.77g/L,其相对分子质量为22.4×2.77=62,去掉2个羟基剩余基团式量为62-17×2=28,故为-C2H4-,则H为HOCH2CH2OH,H与足量D反应生成I为 ,据此解答.
,据此解答.
解答 解:某气态烃A与H2的相对密度为14,Mr(A)=14×2=28,其产量可以用来衡量一个国家的石油化工发展水平,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,C进一步发生氧化反应生成D为CH3COOH,乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3.芳香族化合物F为C、H、O化合物,1mol F与足量NaHCO3溶液反应能生成2mol CO2,则F含有2个羧基,其相对分子质量为166,2个羧基、1个C6H4的总式量为45×2+(12×6+4)=166,则F含有1个苯环、2个羧基,且环上的一氯代物有一种,则F为 ,F与足量的B发生酯化反应生成G为
,F与足量的B发生酯化反应生成G为 ,H为二元醇,其蒸气密度折算成标准状况为2.77g/L,其相对分子质量为22.4×2.77=62,去掉2个羟基剩余基团式量为62-17×2=28,故为-C2H4-,则H为HOCH2CH2OH,H与足量D反应生成I为
,H为二元醇,其蒸气密度折算成标准状况为2.77g/L,其相对分子质量为22.4×2.77=62,去掉2个羟基剩余基团式量为62-17×2=28,故为-C2H4-,则H为HOCH2CH2OH,H与足量D反应生成I为 ,
,
(1)G为 ,其分子式为C12H14O4,故答案为:C12H14O4;
,其分子式为C12H14O4,故答案为:C12H14O4;
(2)反应⑥的化学方程式为:2CH3COOH+HOCH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O,
故答案为:2CH3COOH+HOCH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O;
(3) 与HOCH2CH2OH发生缩聚反应生成高分子化合物,该化学反应方程式为:
与HOCH2CH2OH发生缩聚反应生成高分子化合物,该化学反应方程式为: ,
,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,根据反应条件及某些物质结构简式、题给信息进行推断,正确判断各物质结构简式是解本题关键,注意发生缩聚反应方程式书写特点,易错点是水计量数的判断.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 | |
| B. | 用洁净铁丝蘸取两种样品在酒精灯火焰上灼烧,火焰颜色呈黄色的是小苏打 | |
| C. | 分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打 | |
| D. | 先将两样品配成溶液,后分别加入石灰水,无白色沉淀生成的是小苏打 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

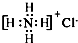
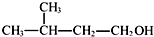
| A. | ①②③ | B. | ③④ | C. | ②④⑤ | D. | ①④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
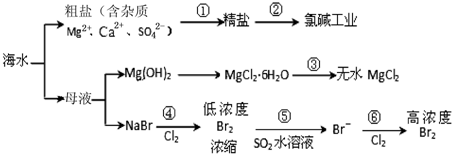
| A. | 除去粗盐中杂质(Mg2+、Ca2+、SO42-),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 在过程③中将MgCl2•6H2O灼烧即可制得无水MgCl2 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br- 需消耗2.24 L Cl2 | |
| D. | 从第④步到第⑥步的目的是为了浓缩富集溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com