
| V |
| Vm |
| n |
| V |
| 2.24L |
| 22.4L/mol |
| 18.6g-10.6g |
| 40g/mol |
| 0.4mol |
| 0.5L |


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
| 实验步骤 | 预期现象及结论 |
| 步骤1:取少量固体分别于试管中,加入一定量的蒸馏水溶解 | 固体全部溶解则没有S生成 |
| 步骤2:取少许液体加HCl | |
| 步骤3 取少许液体加HCl和BaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 9 |
| 4 |
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
| A、反应开始时,丙中的反应速率最快,乙中的反应速率最慢 |
| B、平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L |
| C、平衡时,甲中和丙中H2的转化率均是60% |
| D、平衡时,乙中CO2的转化率大于60% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中,三种金属中有两种金属过量 |
| B、参加反应的金属Na、Mg、Al的物质的量之比为6:3:2 |
| C、镁的物质的量为0.1mol |
| D、V=2.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1mol/L氨水 |
| B、图②表示常温下,等量锌粉分别与两份足量的等体积等浓度的盐酸反应 |
| C、图③表示向CaCl2溶液中通入CO2 |
| D、图④表示向醋酸溶液中滴入氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
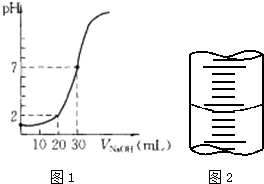 用一定物质的量浓度的NaOH溶液滴定10.00mL已知浓度的盐酸,滴定结果如图1所示.回答下列问题:
用一定物质的量浓度的NaOH溶液滴定10.00mL已知浓度的盐酸,滴定结果如图1所示.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4 L H2O含有的分子数为1 NA |
| B、100mL0.1mol/L Na2CO3溶液中含有的Na+离子数为0.1NA |
| C、通常状况下,NA个CO2分子占有的体积为22.4 L |
| D、48gO2和O3的混合气体中氧原子数目为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com