
| A. | 燃烧反应一定是放热反应 | |
| B. | 只要是在点燃条件下进行的反应就一定是吸热反应 | |
| C. | 只要是在常温常压下进行的反应就一定是放热反应 | |
| D. | 如果反应物的总能量低于生成物的总能量,该反应一定是放热反应 |
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:选择题

| A. | W元素原子得电子能力比Z的弱 | |
| B. | 元素W的最高价氧化物对应的水化物是强酸 | |
| C. | 元素Y的原子半径在同周期主族元素中最大 | |
| D. | 元素Z的气态氢化物的稳定性在同主族元素中最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状态下,1L庚烷完全燃烧后,所生成的气态产物的分子数为$\frac{7}{22.4}$ NA | |
| B. | 1 mol碳正离子CH5+所含的电子数为10NA | |
| C. | 标准状态下,16 g甲烷完全燃烧所消耗氧气的分子数为NA | |
| D. | 0.5 mol C3H8分子中含C-H共价键2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 在20~25min之间,pH=10时R的平均降解速率为0.04 mol•L-1•min-1 | |
| B. | 溶液酸性越强,R的降解速率越小 | |
| C. | R的起始浓度越小,降解速率越大 | |
| D. | 50min时,pH=2和pH=7时R的降解百分率相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
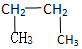
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷与氯气取代 | B. | 乙烯与氢气加成,再用氯气取代 | ||
| C. | 乙烯与氯化氢加成 | D. | 乙烯与氯气加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液中可能大量存在:Al3+、NH4+、Cl-、S2- | |
| B. | 0.1 mol/LFeCl3溶液中大量存在:Fe2+、NH4+、SCN-、SO42- | |
| C. | 加入Al粉产生H2的溶液中可能大量存在:K+、Na+、NO3-、Cl- | |
| D. | 中性溶液中可能大量存在:Fe3+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 X、Y、Z、W是中学常见的四种短周期元素,其原子序数依次增大,且原子核外最外层电子数都不少于2,X的族序数与最外层电子数相等.四种元素的单质均能在氧气中燃烧,生成四种相对分子质量都大于26的氧化物,其中有两种氧化物能溶于稀硫酸,三种能溶于烧碱溶液.四种元素单质的混合物有如下性质:下列说法正确的是( )
X、Y、Z、W是中学常见的四种短周期元素,其原子序数依次增大,且原子核外最外层电子数都不少于2,X的族序数与最外层电子数相等.四种元素的单质均能在氧气中燃烧,生成四种相对分子质量都大于26的氧化物,其中有两种氧化物能溶于稀硫酸,三种能溶于烧碱溶液.四种元素单质的混合物有如下性质:下列说法正确的是( )| A. | 原子半径:X>Y>Z>W | |
| B. | 简单气态氮化物的热稳定性:W>X | |
| C. | 最高价氧化物对应的水化物的碱性:Z>Y | |
| D. | X和W组成的化合物常作砂纸、砂轮的磨料 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com