
| 20.02mL+19.98mL |
| 2 |
| 0.56g |
| 5g |
| 20.02mL+19.98mL |
| 2 |
| 0.56g |
| 5g |


科目:高中化学 来源: 题型:
| A、密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ?mol-1 |
| B、稀醋酸与0.1 mol?L-1 NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ?mol-1 |
| C、已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ?mol-1 |
| D、已知2C(s)+O2(g)=2CO(g)△H=-221 kJ?mol-1,则可知C的燃烧热△H=-110.5 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铝溶液中加入过量氨水 Al3++3OH-=Al(OH)3↓ | ||||
B、电解饱和食盐水 2Cl-+2H+
| ||||
| C、在稀氨水中通入过量CO2 NH3?H2O+CO2=NH4++HCO3- | ||||
| D、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
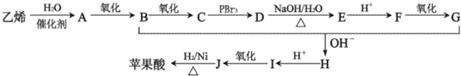
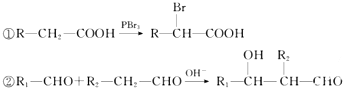
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) | c(S
| c(Fe2+、Fe3+) | ||
| O | 2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
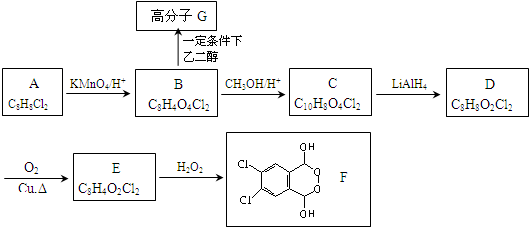
| LiAlH4 |
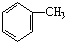
| KMnO4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
 某烧碱溶液中含有少量杂质(不与盐酸反应),现用标准盐酸滴定NaOH溶液,测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用标准盐酸滴定NaOH溶液,测定其浓度.| 滴定序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | ||
| 滴定前 | 滴定后 | 消耗的体积 | ||
| 1 | V | 0.50 | 25.80 | 25.30 |
| 2 | V | |||
| 3 | V | 6.00 | 31.35 | 25.35 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com