
臭氧与KI溶液反应,生成一种可使带余烬的木条复燃的气体,向反应后溶液中加入酚酞试液变红,加入淀粉溶液后变蓝。空气中臭氧含量超过10-5%(体积分数)时,会对人体造成伤害。为测定某房间内空气中臭氧的含量,将0 ℃、1.01×105 Pa下的33.6 m3的空气通入KI溶液,使之完全反应,在所得溶液中加入0.01 mol·L-1 Na2S2O3溶液60 mL恰好完全反应:2Na2S2O3+I2====Na2S4O6+2NaI
(1)完成O3与KI反应的化学方程式。
(2)计算空气中臭氧的体积分数。
(3)该房间内空气中的臭氧是否对人体有害?
科目:高中化学 来源: 题型:
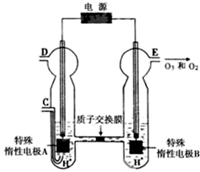 (2011?重庆)臭氧是一种强氧化剂,常用于消毒、灭菌等.
(2011?重庆)臭氧是一种强氧化剂,常用于消毒、灭菌等.| pH t/min T/℃ |
3.0 | 4.0 | 5.0 | 6.0 |
| 20 | 301 | 231 | 169 | 58 |
| 30 | 158 | 108 | 48 | 15 |
| 50 | 31 | 26 | 15 | 7 |
| x-2y |
| y |
| x-2y |
| y |
查看答案和解析>>
科目:高中化学 来源:101网校同步练习 高一化学 山东科学技术出版社 鲁教版 题型:038
空气中含有少量臭氧(O3)可以起到消毒、杀菌的作用.但臭氧过量会对人体有害.我国的环境空气质量标准对空气中臭氧的最高浓度(单位体积的空气中所含臭氧的质量)限值如下表所示:
臭氧与KI溶液反应,生成1种可使带火星木条复燃的气体,反应后的溶液能使酚酞试液变红,也能使蘸有淀粉溶液的滤纸条变蓝.为测定某地臭氧的含量,将50m3的空气通过足量的KI溶液,使臭氧完全反应:在所得溶液中再加入适量的硫代硫酸钠(Na2S2O3)溶液(含Na2S2O3的质量为47.4 mg).恰好完全反应(2Na2S2O3+I2![]() Na2S4O6+2NaI).
Na2S4O6+2NaI).
(1)O3与KI反应的化学方程式:_________________________.
(2)通过计算确定该地区空气中臭氧浓度的级别.
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)完成O3与KI反应的化学方程式。
(2)计算空气中臭氧的体积分数。
(3)该房间内空气中的臭氧是否对人体有害?
查看答案和解析>>
科目:高中化学 来源: 题型:
臭氧与KI溶液反应,生成一种可使带余烬的木条复燃的气体,向反应后溶液中加入酚酞试液变红,加入淀粉溶液后变蓝。空气中臭氧含量超过10-5%(体积分数)时,会对人体造成伤害。为测定某房间内空气中臭氧的含量,将0 ℃、1.01×105 Pa下的33.6 m3的空气通入KI溶液,使之完全反应,在所得溶液中加入0.01 mol·L-1 Na2S2O3溶液60 mL恰好完全反应:2Na2S2O3+I2====Na2S4O6+2NaI
(1)完成O3与KI反应的化学方程式。
(2)计算空气中臭氧的体积分数。
(3)该房间内空气中的臭氧是否对人体有害?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com