
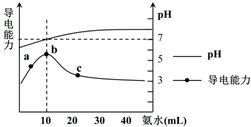
| A. | a~b点导电能力增强说明HR为弱酸 | |
| B. | b点溶液pH=7说明NH4R没有水解 | |
| C. | c 点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+) | |
| D. | b-c任意点溶液均有c(H+)•c(OH-)=Kw=1.0×10-14 mol2•L-2 |
分析 A.溶液导电能力与离子浓度成正比,如果HR是强电解质,加入氨水至溶液呈中性时,溶液中离子浓度会减小,导致溶液导电能力降低;
B.弱离子在水溶液中会发生水解反应;
C.c点溶液的pH>7,说明溶液呈碱性,溶液中c(OH-)>c(H+),再结合电荷守恒判断;
D.离子积常数只与温度有关,温度不变,离子积常数不变.
解答 解:A.溶液导电能力与离子浓度成正比,如果HR是强电解质,加入氨水至溶液呈中性时,溶液中离子浓度会减小,导致溶液导电能力降低,根据图知,加入氨水至溶液呈中性时随着氨水的加入,溶液导电能力增强,说明离子浓度增大,则HR为弱电解质,故A正确;
B.弱离子在水溶液中会发生水解反应,根据A知,HR是弱电解质,且一水合氨是弱电解质,所以NH4R是弱酸弱碱盐,b点溶液呈中性,且此时二者的浓度、体积都相等,说明HR和一水合氨的电离程度相等,所以该点溶液中铵根离子和酸根离子水解程度相等,故B错误;
C.c点溶液的pH>7,说明溶液呈碱性,溶液中c(OH-)>c(H+),再结合电荷守恒得c(NH4+)>c(R-),故C正确;
D.离子积常数只与温度有关,温度不变,离子积常数不变,所以b-c任意点溶液均有c(H+)•c(OH-)=Kw=1.0×10-14 mol2•L-2,故D正确;
故选B.
点评 本题考查酸碱混合溶液定性判断,为高频考点,明确图中曲线变化趋势及曲线含义是解本题关键,侧重考查学生分析判断及知识综合运用能力,易错选项是D,注意:离子积常数只与温度有关,与溶液浓度及酸碱性无关,题目难度中等.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.0004mol/(L•min) | B. | 0.0002mol/(L•s) | C. | 0.0016 | D. | 0.012 mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 待测盐酸体积(mL) | 滴入Na2CO3溶液体积(mL) |
| 1 | 20.00 | 18.80 |
| 2 | 20.00 | 16.95 |
| 3 | 20.00 | 17.05 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/mol | ||
| CO | H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径 (10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 | 1.02 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | +6 | +1 | |
| -2 | -3 | -1 | -3 | -2 |
 ;
;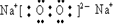 .
. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无机非金属材料中不可能含有金属元素 | |
| B. | 铝盐、铁盐有净水作用,向浑浊的水中加入少量明矾或硫酸铁溶液,搅拌,过一段时间,水的底部会出现很多絮状不溶物,水变澄清透明 | |
| C. | 氯化物在化学工业领域有重要应用,例如SiCl4、GeCl4、TiCl4分别是制取高纯硅、锗和钛的重要中间物质 | |
| D. | 地球上存在的天然二氧化硅形态有结晶形和无定形两大类统称硅石 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com