
| A. | NaHSeO4溶液和Na2SeO4溶液均显碱性 | |
| B. | pH=3的H2SeO4和NaHSeO4溶液,后者水的电离程度大 | |
| C. | H2SeO4溶液中滴加少量氨水的离子方程式:H++NH3•H2O=NH4++H2O | |
| D. | Na2CO3溶液中加入少量H2SeO4的离子方程式为:CO32-+H+=HCO3- |
分析 A.H2SeO4=H++HSeO4-,第一步完全电离,HSeO4-不水解;
B.pH=3的H2SeO4和NaHSeO4溶液,氢离子浓度相同,对水的电离影响程度相同;
C.H2SeO4溶液中滴加少量氨水反应生成酸式盐NaHSeO4,H2SeO4=H++HSeO4-,第一步完全电离;
D.已知HSeO4-?H++SeO42-,K2=1.2×10-2大于H2CO3的一级电离常数分别为Kl=4.2×10-7,所以KHCO3和KHSeO4两溶液混合,强酸制弱酸生成二氧化碳不能存在.
解答 解:A.H2SeO4=H++HSeO4-,第一步完全电离,HSeO4-不水解,NaHSeO4溶液显酸性,Na2SeO4溶液显碱性,故A错误;
B.pH=3的H2SeO4和NaHSeO4溶液,氢离子浓度相同,对水的电离影响程度相同,水的电离程度相同,故B错误;
C.H2SeO4溶液中滴加少量氨水反应生成酸式盐NaHSeO4,H2SeO4=H++HSeO4-,第一步完全电离,氨水少量所以第一步完全电离产生的氢离子,还过量,H2SeO4溶液中滴加少量氨水的离子方程式:H++NH3•H2O=NH4++H2O,故C正确;
D.已知HSeO4-?H++SeO42-,K2=1.2×10-2大于H2CO3的一级电离常数分别为Kl=4.2×10-7,所以HCO3-和HSeO4-两溶液混合,强酸制弱酸不能共存,所以反应方程式为:CO32-+H2SeO4-=CO2↑+SeO42-+H2O,故D错误;
故选C.
点评 本题考查较为综合,涉及物质的量程度分析、产物判断、电离平衡常数比较等知识,题目难度中等,注意判断反应物和生成物,用守恒的方法和原理书写离子方程式.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 氧化物 | B. | 有机物 | C. | 酸 | D. | 盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 取一定量固体,溶解,向溶液中通入足量的CO2,观察到有晶体析出,说明原固体中一定含有 Na2CO3 | |
| B. | 取一定量固体,溶解,向溶液中加人适量CaO粉末,充分反应后观察到有白色沉淀生成,说明 原固体中一定含有Na2CO3 | |
| C. | 取一定量固体,溶解,向溶液中滴加适量AgNO3溶液后有白色沉淀生成,这个现象不能说明原固体中一定含有NaCl | |
| D. | 称取3.80g固体,加热至恒重,质量减少了 0.620g.用足童稀盐酸溶解残留固体,充分反应后,收集到0.880g气体,说明原固体中仅含有Na2CO3和NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+ | B. | SO32- | C. | SiO32- | D. | Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
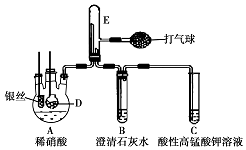 某化学实验小组利用如图装置证明银和稀硝酸反应产生NO,D是内置块状大理石的多孔玻璃笼.(加热装置和夹持装置均已略去.
某化学实验小组利用如图装置证明银和稀硝酸反应产生NO,D是内置块状大理石的多孔玻璃笼.(加热装置和夹持装置均已略去.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{92}^{235}$U与${\;}_{92}^{238}$U互为同素异形体 | |
| B. | ${\;}_{92}^{235}$U与${\;}_{92}^{238}$U互为同位素 | |
| C. | ${\;}_{92}^{235}$U原子核中含有92个中子 | |
| D. | ${\;}_{92}^{235}$U原子核外有143个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com