
【题目】CO是火力发电厂释放出的主要尾气,为减少对环境污染,发电厂试图采用CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2 , 在催化剂的作用下发生反应:CO(g)+Cl2(g)COCl2(g)△H=a kJ/mol
反应过程中测定的部分数据如表:
t/min | n (CO)/mol | n (Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
(1)比较各时段平均速率v(COCl2):v(0﹣1)v(0﹣2);v(0﹣2)v(1﹣2) (填“>”、“=”或“<”).
(2)在2min~4min间,v(Cl2)正v(Cl2)逆 (填“>”、“=”或“<”),该温度下K=
(3)已知X、L可分别代表温度或压强,如图表示L一定时,CO的砖化率随X的变化关系.
X代表的物理量是;a0 (填“>”,“=”,“<”),依据是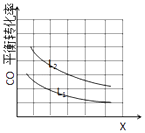
【答案】
(1)>;>
(2)=;5
(3)温度;<;因为X增大时,CO的平衡转化率降低,平衡逆向移动
【解析】解:(1)由表中数据,0﹣1min内,△n(CO)=1.2mol﹣0.9mol=0.3mol,由方程式可知△c(COCl2)=△c(CO)=0.3mol,则v(COCl2)= ![]() =0.15mol/(L.min),0~2min内△n(CO)=1.2mol﹣0.8mol=0.4mol,由方程式可知△c(COCl2)=△c(CO)=0.4mol,则v(COCl2)=
=0.15mol/(L.min),0~2min内△n(CO)=1.2mol﹣0.8mol=0.4mol,由方程式可知△c(COCl2)=△c(CO)=0.4mol,则v(COCl2)= ![]() 0.1mol/(L.min),1min﹣2min内,△n(CO)=0.9mol﹣0.8mol=0.1mol,由方程式可知△c(COCl2)=△c(CO)=0.1mol,则v(COCl2))=△c(CO)=
0.1mol/(L.min),1min﹣2min内,△n(CO)=0.9mol﹣0.8mol=0.1mol,由方程式可知△c(COCl2)=△c(CO)=0.1mol,则v(COCl2))=△c(CO)= ![]() =0.05mol/(L.min),v(0﹣1)>v(0﹣2);v(0﹣2)>v(1﹣2) , 故答案为:>;>;(2)4min内,反应的氯气为0.6mol﹣0.2mol=0.4mol,由方程式可知参加反应的CO为0.4mol,故4min时CO为1.2mol﹣0.4mol=0.8mol,与2min时CO的物质的量相等,则2min、4min处于平衡状态,在2min~4min间,v(Cl2)正 =v(Cl2)逆 ,
=0.05mol/(L.min),v(0﹣1)>v(0﹣2);v(0﹣2)>v(1﹣2) , 故答案为:>;>;(2)4min内,反应的氯气为0.6mol﹣0.2mol=0.4mol,由方程式可知参加反应的CO为0.4mol,故4min时CO为1.2mol﹣0.4mol=0.8mol,与2min时CO的物质的量相等,则2min、4min处于平衡状态,在2min~4min间,v(Cl2)正 =v(Cl2)逆 ,
由方程式可知,平衡时生成COCl2为0.4mol,该温度下平衡常数K= ![]() =
= ![]() =5,
=5,
故答案为:=;5;(3)正反应为气体体积减小的反应,增大压强平衡正向移动,CO转化率增大,而图中随X增大时,CO的平衡转化率降低,平衡逆向移动,则X为温度,正反应为放热反应,故a<0,
故答案为:温度;<;因为X增大时,CO的平衡转化率降低,平衡逆向移动.
(1)根据v= ![]() 计算v(COCl2)比较大小;(2)4min内,反应的氯气为0.6mol﹣0.2mol=0.4mol,由方程式可知参加反应的CO为0.4mol,故4min时CO为1.2mol﹣0.4mol=0.8mol,与2min时CO的物质的量相等,则2min、4min处于平衡状态;
计算v(COCl2)比较大小;(2)4min内,反应的氯气为0.6mol﹣0.2mol=0.4mol,由方程式可知参加反应的CO为0.4mol,故4min时CO为1.2mol﹣0.4mol=0.8mol,与2min时CO的物质的量相等,则2min、4min处于平衡状态;
由方程式可知,平衡时生成COCl2为0.4mol,平衡常数K= ![]() ;(3)正反应为气体体积减小的反应,增大压强平衡正向移动,CO转化率增大,而图中随X增大时,CO的平衡转化率降低,平衡逆向移动,则X为温度,正反应为放热反应.
;(3)正反应为气体体积减小的反应,增大压强平衡正向移动,CO转化率增大,而图中随X增大时,CO的平衡转化率降低,平衡逆向移动,则X为温度,正反应为放热反应.


科目:高中化学 来源: 题型:
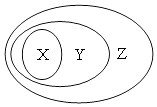
【题目】用下图表示的一些物质或概念间的从属关系中不正确的是( )
X | Y | Z | |
A | 氧化物 | 化合物 | 纯净物 |
B | 氯化钠 | 电解质 | 化合物 |
C | 金属氧化物 | 碱性氧化物 | 氧化物 |
D | 牛奶 | 胶体 | 分散系 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组欲鉴定某硫酸钠样品中是否含有亚硫酸钠,设计方案如下:取少量固体配成溶液,往溶液中滴加少量酸性KMnO4溶液,观察溶液是否褪色.如果溶液紫色褪去,说明该样品中含有亚硫酸钠. 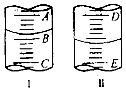
(1)用离子方程式表示该反应原理: .
(2)图I表示100mL量筒中液面的位置,A与B,B与C刻度间相差10mL,如果刻度A为30,量筒中液体的体积是mL.图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填字母)
A.等于amL B.等于(25﹣a)mL C.大于amL D.大于(25﹣a)mL
(3)该小组同学欲测定样品中亚硫酸钠的含量,操作步骤如下:
a.称取mg样品,用蒸馏水溶解并置于锥形瓶中
b.将V1mL C1mol/L的酸性KMnO4溶液(过量)倒入锥形瓶中振荡
c.用C2mol/L草酸钠(Na2C2O4)溶液滴定过量的KMnO4 , 至滴定终点时用去Na2C2O4溶液V2mL
①KMnO4溶液应装在式滴定管中,达到滴定终点时溶液颜色的变化 .
②样品中Na2SO3的物质的量为mol.(用含C1、V1、C2、V2的代数式表示).
(4)下列操作会导致测得的Na2SO3的物质的量偏高的是(填字母,双选).
A.未用Na2C2O4标准液润洗滴定管
B.滴定前仰视盛有Na2C2O4溶液的滴定管,滴定后俯视
C.滴定前滴定管尖嘴处有气泡,滴定后消失
D.滴定时摇动锥形瓶,瓶中的液滴溅出.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,氧化铁可以与一氧化碳发生下列反应:Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g)
(1)①该反应的平衡常数表达式为:K= .
②该温度下,在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成了单质铁11.2g.则10min内CO的平均反应速为 .
(2)说明该反应已达到平衡状态: .
a.CO或(CO2)的生成速率与消耗速率相等;
b.CO(或CO2)的质量不再改变
c.CO(或CO2)的体积分数50%
(3)I2O5可使H2S、CO、HCl等氧化,常用于定量测定CO的含量.已知:
2I2(s)+5O2(g)=2I2O5(s)△H1=﹣75.56kJmol﹣1
2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJmol﹣1
写出CO(g)与I2O5(s)反应生成I2(s)和CO2(g)的热化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了将混有Na2SO4、NaHCO3的NaCl固体提纯,制得纯净的氯化钠溶液,某学生设计了如图所示的实验方案: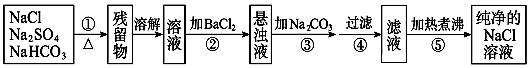
已知碳酸氢钠在加热条件下能分解成碳酸钠、二氧化碳和水,而NaCl和Na2SO4固体加热时不发生化学变化.请回答下列问题:
(1)操作①盛放药品可选用(填仪器名称).
(2)操作②为什么不用Ba(NO3)2溶液,其理由是: .
(3)进行操作②后,判断SO42﹣已除尽的方法是: .
(4)操作③的目的是: .
(5)此设计方案是否严密(填“是”或“否”)理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析城市空气样本,主要污染物为可吸入颗粒物pm2.5、NOx、SO2等,其主要来源为燃煤和机动车尾气排放等.
(1)某同学为检测样本中所含成份,将样本用蒸馏水处理制成待测试样,设计实验及实验现象如图:
①该实验能确认存在的阳离子是 .
②该实验检测出样本中有NO3﹣ , 根据是(用化学方程式解释) .
③根据该实验能否确定样本中含有SO32﹣ , (填“能”或“否”),若要确定SO32﹣ , 所需的实验药品可以是 .
(2)PM2.5是指大气中直径小于或等于2.5μm(1μm=103nm)的颗粒物.下列说法不正确的是(填字母序号).
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(3)科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和Ca(NO2)2 . 
①CaSO4可以调节水泥的硬化时间.尾气中SO2与石灰乳反应生成CaSO4的化学方程式为 .
②Ca(NO2)2可制成混凝土防冻剂、钢筋阻锈剂等.尾气中NO、NO2与石灰乳反应生成Ca(NO2)2的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.126C和146C是2种核素,他们互称同位素
B.近期化学研究者开发出被称为第五形态的固体碳,这种新的碳结构称作“纳米泡沫”,它外形类似海绵,比重极小,并具有磁性.纳米泡沫碳与C60互称同素异形体
C.![]() 与
与  互为同分异构体
互为同分异构体
D.硝基苯可看成是由 ![]() 和﹣NO2两种基团组成
和﹣NO2两种基团组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关药品的保存和使用不正确的是( )
A.溴水盛于带磨砂玻璃塞的细口瓶中
B.硫酸铜粉末、氯化钙等药品贮存于干燥器中
C.白磷需浸入水中密封保存
D.用碳酸钠滴定盐酸时,Na2CO3液应盛于酸式滴定管中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于电解NaCl水溶液的说法正确的是 ( )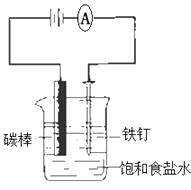
①电解产物为Cl2和Na
②电解过程中,碳棒一极产生黄绿色气体
③电解一段时间后,在碳棒附近的溶液中滴加酚酞溶液,溶液呈红色
④电解一段时间后,在铁钉附近的溶液中滴加酚酞溶液,溶液呈红色
A.①③
B.①④
C.②③
D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com