
| A�� | 2 Q2=Q1 | B�� | 2 Q2��Q1 | C�� | 2 Q2��Q1��Q | D�� | Q=Q1��Q2 |
���� 2SO2��g��+O2��g��?2SO3��g����H=-QkJ/mol����ʾ������������2mol SO2��1molO2��ȫ��Ӧ����1molSO3����ų�����ΪQkJ���ٽ�Ͽ��淴Ӧ�з�Ӧ�ﲻ����ȫ��Ӧ�����ʵ�����ų������������ȡ�ƽ���ƶ��Ƚ��
��� �⣺��Ӧ���Ȼ�ѧ����ʽΪ��2SO2��g��+O2��g��?2SO3��g����H=-Q kJ/mol��
���Ȼ�ѧ����ʽ��֪�������������·�Ӧ����2molSO3�������Q kJ������2mol SO2��1molO2�����ɵ�����������С��2mol������Q1��Q kJ��
ͨ��1mol SO2��0.5molO2�����ת���������2mol SO2��1molO2��ͬ�������Ϊ$\frac{{Q}_{1}}{2}$kJ�����Ǵ�ʱ��ϵѹǿ�ȼ���2mol SO2��1molO2ҪС������ƽ��������ƶ�������ʵ�ʷų���������$\frac{{Q}_{1}}{2}$kJ����2Q2��Q1�����ϵã�2Q2��Q1��Q kJ��
��ѡC��
���� ���⿼��ƽ���ƶ�����Ӧ�ȵļ��㣬��Ŀ�Ѷ��еȣ�����ע��Ũ�ȶ�ƽ���Ӱ���Լ����淴Ӧ��������


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 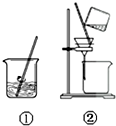 ��ȥ��������м������� | B�� |  ʵ������ȡ�������� | ||
| C�� |  ʵ��������ϩ | D�� |  ����ƾ���ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4.6 g C7H8��C3H8O3�Ļ������������ԭ������Ϊ0.4NA | |
| B�� | ��״���£�11.2 L C2H5OH�������ķ�����Ϊ0.5NA | |
| C�� | ���³�ѹ�£�0.1 mol Na2O2��CO2��Ӧת�Ƶĵ�����ĿΪ0.4NA | |
| D�� | ��1 L 0.1 mol•L-1̼������Һ�У���������������0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ơ��ƿ���д��������ݳ� | |
| B�� | ���ڷ�ӦI2��g��+H2��g��?2HI��g���ﵽƽ�������ѹǿ������ɫ���� | |
| C�� | ��ɫCoCl2��Һ��������Һ��ɫ��Ϊ��ɫ���ñ�ˮ��ȴ��Һ��ɫ��Ϊ�ۺ�ɫ | |
| D�� | ��ҵ�ϳɰ���N2��g��+3H2��g��?2NH3��g����H=-92.4 kJ/mol��ѡ���ѹ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������������� | B�� | �����������ʵ�����ˮ�� | ||
| C�� | ��Һ���ʵ���Ũ����� | D�� | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������ͼװ�ã���Ҫ��ش����⣮
������ͼװ�ã���Ҫ��ش����⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com