
ЎѕМвДїЎїЈЁ1Ј©КµСйІвµГ16 gјЧґјCH3OH(l)ФЪСхЖшЦРід·ЦИјЙХЙъіЙ¶юСх»ЇМјЖшМеєНТєМ¬Л®К±КН·Еіц363.25 kJµДИИБїЈ¬КФРґіцјЧґјИјЙХµДИИ»ЇС§·ЅіМКЅЈє ____________________ЎЈ
ЈЁ2Ј©єПіЙ°±·ґУ¦N2(g)Ј«3H2(g) ![]() 2NH3(g)¦¤HЈЅa kJЎ¤molЈ1Ј¬·ґУ¦№эіМµДДЬБї±д»ЇИзНјЛщКѕЈє
2NH3(g)¦¤HЈЅa kJЎ¤molЈ1Ј¬·ґУ¦№эіМµДДЬБї±д»ЇИзНјЛщКѕЈє
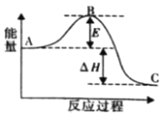
ўЩёГ·ґУ¦НЁіЈУГМъЧчґЯ»ЇјБЈ¬јУґЯ»ЇјБ»бК№НјЦРE______ЈЁМоЎ°±дґуЎ±»тЎ°±дРЎЎ±Ј©Ј¬EµДґуРЎ¶ФёГ·ґУ¦µД·ґУ¦ИИУРОЮУ°ПмЈї______(МоЎ°УРЎ±»тЎ°ОЮЎ±)ЎЈ
ўЪУР№ШјьДЬКэѕЭИзПВЈє
»ЇС§јь | HЎЄH | NЎЄH | NЎФN |
јьДЬ(kJЎ¤molЈ1) | 436 | 391 | 945 |
КФёщѕЭ±нЦРЛщБРјьДЬКэѕЭјЖЛгaОЄ____________ЎЈ
ЈЁ3Ј©·ўЙдОАРЗК±їЙУГлВЈЁN2H4Ј©ОЄИјБПЈ¬УГ¶юСх»ЇµЄОЄСх»ЇјБЈ¬ХвБЅЦЦОпЦК·ґУ¦ЙъіЙµЄЖшєНЛ®ХфЖшЎЈТСЦЄЈєўЩN2(g)+2O2(g)=2NO2(g) Ўч¦§1=a kJ/mol
ўЪN2H4(g)+O2(g)=N2(g)+2H2O(g) Ўч¦§2=bkJ/mol
РґіцлВєН¶юСх»ЇµЄ·ґУ¦ЙъіЙµЄЖшєНЖшМ¬Л®µДИИ»ЇС§·ЅіМКЅЈє_____________________ЎЈ
Ўѕґр°ёЎїCH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ЎчH=-726.5kJ/mol ±дРЎ ОЮ -93 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ЎчH=(2b-a)kJ/mol
O2(g)=CO2(g)+2H2O(l) ЎчH=-726.5kJ/mol ±дРЎ ОЮ -93 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ЎчH=(2b-a)kJ/mol
ЎѕЅвОцЎї
ЈЁ1Ј©16 gјЧґјµДОпЦКµДБї=![]() Ј¬ЖдИјЙХ·Еіц363.25 kJµДИИБїЈ¬Фт1molјЧґјНкИ«ИјЙХ·ЕіцИИБїОЄ
Ј¬ЖдИјЙХ·Еіц363.25 kJµДИИБїЈ¬Фт1molјЧґјНкИ«ИјЙХ·ЕіцИИБїОЄ![]() Ј¬ёщѕЭИјЙХИИµД¶ЁТеЈ¬ЖдИјЙХµДИИ»ЇС§·ґУ¦·ЅіМКЅОЄЈєCH3OH(l)+
Ј¬ёщѕЭИјЙХИИµД¶ЁТеЈ¬ЖдИјЙХµДИИ»ЇС§·ґУ¦·ЅіМКЅОЄЈєCH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) ЎчH=-726.5kJ/molЈ»
O2(g)=CO2(g)+2H2O(l) ЎчH=-726.5kJ/molЈ»
ЈЁ2Ј©ўЩґЯ»ЇјБДЬЅµµН·ґУ¦ЛщРи»о»ЇДЬЈ¬µ«І»У°ПммК±дµДґуРЎЈ¬№Кґр°ёОЄЈє±дРЎЈ¬ОЮЈ»
ўЪЎчH=·ґУ¦ОпµДЧЬјьДЬЦ®єН-ЙъіЙОпµДЧЬјьДЬЦ®єНЈ¬Фт![]() Ј¬№Кґр°ёОЄЈє93Ј»
Ј¬№Кґр°ёОЄЈє93Ј»
ЈЁ3Ј©АыУГёЗЛ№¶ЁВЙЈ¬![]() јґїЙµГµЅДї±кИИ»ЇС§·ґУ¦·ЅіМКЅЈ¬јґ2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ЎчH=(2b-a)kJ/molЎЈ
јґїЙµГµЅДї±кИИ»ЇС§·ґУ¦·ЅіМКЅЈ¬јґ2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ЎчH=(2b-a)kJ/molЎЈ


 У¦УГМвЧчТµ±ѕПµБРґр°ё
У¦УГМвЧчТµ±ѕПµБРґр°ё КојЩЧчТµКојЩїмАЦБ·Оч°Ііц°жЙзПµБРґр°ё
КојЩЧчТµКојЩїмАЦБ·Оч°Ііц°жЙзПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїіфСхКЗАнПлµДСМЖшНСПхКФјБЈ¬ЖдНСПх·ґУ¦ОЄ2NO2(g)+O3(g)![]() N2O5(g)+O2(g)ЎЈПтјЧЎўТТБЅёцМе»э¶јОЄ1.0LµДєгИЭГЬ±ХИЭЖчЦРѕщідИл2.0molNO2єН1.0molO3Ј¬·Ц±рФЪT1ЎўT2ОВ¶ИПВЈ¬ѕ№эТ»¶ОК±јдєуґпµЅЖЅєвЎЈ·ґУ¦№эіМЦРn(O2)ЛжК±јд(t)±д»ЇЗйїцјыПВ±нЎЈПВБРЛµ·ЁІ»ХэИ·µДКЗЈЁ Ј©
N2O5(g)+O2(g)ЎЈПтјЧЎўТТБЅёцМе»э¶јОЄ1.0LµДєгИЭГЬ±ХИЭЖчЦРѕщідИл2.0molNO2єН1.0molO3Ј¬·Ц±рФЪT1ЎўT2ОВ¶ИПВЈ¬ѕ№эТ»¶ОК±јдєуґпµЅЖЅєвЎЈ·ґУ¦№эіМЦРn(O2)ЛжК±јд(t)±д»ЇЗйїцјыПВ±нЎЈПВБРЛµ·ЁІ»ХэИ·µДКЗЈЁ Ј©
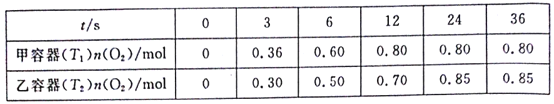
A.T1ЈјT2
B.ёГ·ґУ¦ЎчHЈј0
C.јЧИЭЖчФЪОВ¶ИОЄT1К±µДЖЅєвіЈКэОЄ20molЎ¤L-1
D.ТТИЭЖчЦРЈ¬0Ў«3sДЪµДЖЅѕщ·ґУ¦ЛЩВКv(NO2)=0.2molЎ¤L-1Ў¤s-1
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїXЎўYЎўZЎўWЎўQЎўR КЗЦЬЖЪ±нЦРЗ° 36 єЕФЄЛШЈ¬єЛµзєЙКэТАґОФцґуЈ¬ЖдЦР XЎўYЎўZЎў W ¶јКЗФЄЛШЦЬЖЪ±нЦР¶МЦЬЖЪФЄЛШЎЈX ОЄ·ЗЅрКфФЄЛШЈ¬ЗТ X ФЧУµДєЛНвіЙ¶ФµзЧУКэКЗОґіЙ¶ФµзЧУКэµД 2 ±¶Ј¬Z µДґОНвІгµзЧУКэКЗЧоНвІгµзЧУКэµД![]() Ј¬W ФЧУµД s µзЧУУл p µзЧУКэПаµИЈ¬Q КЗЗ°ЛДЦЬЖЪЦРµзёєРФЧоРЎµДФЄЛШЈ¬R µДФЧУРтКэОЄ 29ЎЈ »ШґрПВБРОКМвЈє
Ј¬W ФЧУµД s µзЧУУл p µзЧУКэПаµИЈ¬Q КЗЗ°ЛДЦЬЖЪЦРµзёєРФЧоРЎµДФЄЛШЈ¬R µДФЧУРтКэОЄ 29ЎЈ »ШґрПВБРОКМвЈє
ЈЁ1Ј©XµДЧоёЯјЫСх»ЇОп¶ФУ¦µДЛ®»ЇОп·ЦЧУЦРЈ¬ЦРРДФЧУІЙИЎ______________ФУ»ЇЎЈ
ЈЁ2Ј©»ЇєПОп XZ Ул Y µДµҐЦК·ЦЧУ»ҐОЄ______________Ј¬1mol XZ ЦРє¬УЦмьµДКэДїОЄ______________ЎЈ
ЈЁ3Ј©W µДОИ¶ЁАлЧУєЛНвУР______________ЦЦФЛ¶ЇЧґМ¬µДµзЧУЎЈWФЄЛШµДµЪТ»µзАлДЬ±ИЖдН¬ЦЬЖЪ ПаБЪФЄЛШµДµЪТ»µзАлДЬёЯЈ¬ЖдФТтКЗЈє_____ЎЈ
ЈЁ4Ј©Q µДѕ§МеЅб№№ИзНјЛщКѕЈ¬ФтФЪµҐО»ѕ§°ыЦР Q ФЧУµДёцКэОЄ______________Ј¬ѕ§МеµДЕдО»КэКЗ______________ЎЈ
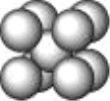
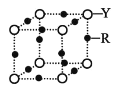
ЈЁ5Ј©RФЄЛШµД»щМ¬ФЧУµДєЛНвµзЧУЕЕІјКЅОЄ________Ј»Y Ул R РОіЙДі ЦЦ»ЇєПОпµДѕ§°ыЅб№№ИзНјЛщКѕЈ¬ТСЦЄёГѕ§МеµДГЬ¶ИОЄ¦СgЎ¤cm-3Ј¬°ў·ьјУµВВЮіЈКэµДКэЦµОЄ NAЈ¬ФтёГѕ§МеЦР R ФЧУєН Y ФЧУЦ®јдµДЧо¶МѕаАлОЄ______________cmЎЈЈЁЦ»РґјЖЛгКЅЈ©
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї¶ФУЪїЙДж·ґУ¦Јє2A(g)+B(g)![]() 2C(g) ¦¤H <0Ј¬ПВБРёчНјЦРХэИ·µДКЗЈЁ Ј©
2C(g) ¦¤H <0Ј¬ПВБРёчНјЦРХэИ·µДКЗЈЁ Ј©
A. B.
B.
C.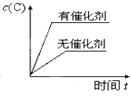 D.
D.
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїБЧ»ЇВБЎўБЧ»ЇРїЎўБЧ»ЇёЖУлЛ®·ґУ¦ІъЙъёЯ¶ѕµДPH3ЖшМеЈЁИЫµгОЄ-132ЎжЈ¬»№ФРФЗїЎўТЧЧФИјЈ©Ј¬їЙУГУЪБёКіС¬ХфЙ±іжЎЈОАЙъ°ІИ«±кЧј№ж¶ЁЈєµ±БёКіЦРБЧ»ЇОпЈЁТФPH3јЖЈ©µДє¬БїµНУЪ0.05mgЎ¤kg-1К±ЛгєПёсЎЈїЙУГТФПВ·Ѕ·ЁІв¶ЁБёКіЦРІРБфµДБЧ»ЇОпє¬БїЈє
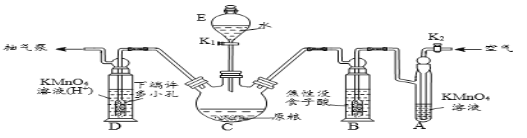
ЈЁІЩЧчБчіМЈ©°ІЧ°ОьКХЧ°ЦГЎъPH3µДІъЙъУлОьКХЎъЧЄТЖKMnO4ОьКХИЬТєЎъСЗБтЛбДЖ±кЧјИЬТєµО¶ЁЎЈ
ЈЁКµСйЧ°ЦГЈ©CЦРКў100 gФБёЈ¬DЦРКўУР 20.00 mL 1.12ЎБ10-4 mol L-1KMnO4ИЬЈЁH2SO4Лб»Ї)ЎЈ
ЈЁ1Ј©ТЗЖчCµДГыіЖКЗ_________Ј»ФБёЧоєГПИґтіЙ·ЫД©Ј¬ЖдФТтКЗ_____________ЎЈ
ЈЁ2Ј©БЧ»ЇёЖУлЛ®·ґУ¦»ЇС§·ЅіМКЅОЄ_____________________________________Ј»јмІйХыМЧЧ°ЦГЖшГЬРФБјєГµД·Ѕ·ЁКЗ_______________________________________ЎЈ
ЈЁ3Ј©AЦРКўЧ°KMnO4ИЬТєµДЧчУГКЗіэИҐїХЖшЦРµД»№ФРФЖшМеЈ»BЦРКўЧ°Ѕ№РФГ»КіЧУЛбµДјоРФИЬТєЈ¬ЖдЧчУГКЗОьКХїХЖшЦРµДO2Ј¬·АЦ№___________Ј»НЁИлїХЖшµДЧчУГКЗ____________ЎЈ
ЈЁ4Ј©DЦРPH3±»Сх»ЇіЙБЧЛбЈ¬Лщ·ўЙъ·ґУ¦µДАлЧУ·ЅіМКЅОЄ_________________________ЎЈ
ЈЁ5Ј©°СDЦРОьКХТєЧЄТЖЦБИЭБїЖїЦРЈ¬јУЛ®ПЎКНЦБ250mLЈ¬ИЎ25.00mLУЪЧ¶РОЖїЦРЈ¬УГ5.0ЎБ10-5mol L-1µДNa2SO3±кЧјИЬТєµО¶ЁКЈУаµДKMnO4ИЬТєЈ¬РґіцёГ·ґУ¦µДАлЧУ·ЅіМКЅ________________Ј¬ПыєД±кNa2SO3ЧјИЬТє11.00mLЈ¬ФтёГФБёЦРБЧ»ЇОпЈЁТФPH3јЖЈ©µДє¬БїОЄ______mg kg-1ЎЈ
ЈЁ6Ј©µО¶ЁЅбКшµДПЦПу_____________________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїФЪёш¶ЁМхјюПВЈ¬ПВБРСЎПоЛщКѕµДОпЦКјдЧЄ»ЇѕщДЬКµПЦµДКЗ
A. NaCl(aq)![]() Cl2(g)
Cl2(g)![]() FeCl2(s)
FeCl2(s)
B. MgCl2(aq)![]() Mg(OH)2(s)
Mg(OH)2(s)![]() MgO (s)
MgO (s)
C. S(s)![]() SO3(g)
SO3(g)![]() H2SO4(aq)
H2SO4(aq)
D. N2(g)![]() NH3(g)
NH3(g)![]() Na2CO3(s)
Na2CO3(s)
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїОЄМбЙэµзіШС»·Р§ВКєНОИ¶ЁРФЈ¬їЖС§јТЅьЖЪАыУГИэО¬¶аїЧєЈГаЧґZnЈЁ3DZnЈ©їЙТФёЯР§іБ»эZnOµДМШµгЈ¬ЙијЖБЛІЙУГЗїјоРФµзЅвЦКµД3DZnЎЄNiOOH¶юґОµзіШЈ¬Ѕб№№ИзПВНјЛщКѕЎЈµзіШ·ґУ¦ОЄZn(s)+2NiOOH(s)+H2O(l)![]() ZnO(s)+2Ni(OH)2(s)ЎЈ
ZnO(s)+2Ni(OH)2(s)ЎЈ

A. ИэО¬¶аїЧєЈГаЧґZnѕЯУРЅПёЯµД±нГж»эЈ¬ЛщіБ»эµДZnO·ЦЙў¶ИёЯ
B. ідµзК±Сфј«·ґУ¦ОЄNi(OH)2(s)+OH(aq)e![]() NiOOH(s)+H2O(l)
NiOOH(s)+H2O(l)
C. ·ЕµзК±ёєј«·ґУ¦ОЄZn(s)+2OH(aq)2e![]() ZnO(s)+H2O(l)
ZnO(s)+H2O(l)
D. ·Еµз№эіМЦРOHНЁ№эёфД¤ґУёєј«ЗшТЖПтХэј«Зш
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїіЈОВПВЈ¬Пт 20 mL 0.1 molЎ¤L-1(NH4)2SO4 ИЬТєЦРЦрµОјУИл 0.2 molЎ¤L-1NaOH ИЬТєК±Ј¬ИЬТєµД pHУлЛщјУ NaOH ИЬТєМе»эµД№ШПµИзНјЛщКѕ(І»їјВЗ»У·ў)ЎЈПВБРЛµ·ЁХэИ·µДКЗ
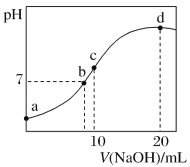
A.µг a ЛщКѕИЬТєЦРЈєc(NH![]() )>c(SO
)>c(SO![]() )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.µг b ЛщКѕИЬТєЦРЈєc(NH![]() )ЈЅc(Na+)>c(H+)ЈЅc(OH)
)ЈЅc(Na+)>c(H+)ЈЅc(OH)
C.µг c ЛщКѕИЬТєЦРЈєc(SO![]() )Ј«c(H+)ЈЅc(NH3Ў¤H2O)Ј«c(OH)
)Ј«c(H+)ЈЅc(NH3Ў¤H2O)Ј«c(OH)
D.µг d ЛщКѕИЬТєЦРЈєc(SO![]() )>c(NH3Ў¤H2O)>c(OH-)>c(NH
)>c(NH3Ў¤H2O)>c(OH-)>c(NH![]() )
)
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї№¤Тµ·ПЖъОпµДЧКФґ»Ї»ШКХФЩАыУГЈ¬їЙТФёьґуПЮ¶ИµШ·ў»УФІДБПµДјЫЦµЎЈДіЅМК¦ФЪЦёµјС§ЙъЧцСРѕїРФС§П°К±Ј¬ДвАыУГ·ПМъРјФЪКµСйКТЦЖ±ёFeSO4ИЬТєЈ¬ФЩУлµИОпЦКµДБїµД(NH4)2SO4·ґУ¦Ј¬ЦЖ±ёІ№СЄјББтЛбСЗМъп§ѕ§Ме[(NH4)2Fe(SO4)2Ў¤6H2OЈ¬Па¶Ф·ЦЧУЦКБїОЄ392]ЎЈБтЛбСЗМъп§ѕ§Ме±ИТ»°гСЗМъСООИ¶ЁЈ¬ФЪїХЖшЦРІ»ТЧ±»Сх»ЇЈ¬ТЧИЬУЪЛ®Ј¬І»ИЬУЪТТґјЎЈ
(1)·ПМъРјµДѕ»»ЇЈєЅ«·ПМъРјН¶Ил10%µДМјЛбДЖИЬТєЦРІўјУИИ5~10minЈ¬НЁ№эЗгОц·ЁЖъИҐґїјоИЬТєЈ¬ІўУГХфБуЛ®Пґѕ»·ПМъРјЈ¬ґэУГЎЈ
(2)ЛбЅюѕ»»ЇєуµД·ПМъРјЈєЅ«2gFe·ЫЎў10mL3molЎ¤L-1µДH2SO4ИЬТєјУИлЙХЖїЦР·ґУ¦Ј¬УГИзНјЛщКѕЧ°ЦГЦЖ±ёFeSO4ИЬТєЎЈ±ЈіЦОВ¶И70~80ЎжЈ¬ККµ±МнјУЛ®ТФІ№ід±»Хф·ўµфµДЛ®·ЦЈ¬ІўїШЦЖИЬТєµДpHЈ¬ЦБ·ґУ¦ОЮГчПФЖшЕЭІъЙъЈ¬НЈЦ№јУИИЈ¬№эВЛЈ¬іЖБїІРБф№ММеЦКБїЎЈ
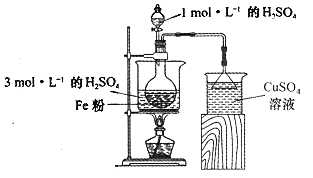
ўЩ·ґУ¦№эіМЦР»бІъЙъЙЩБїH2SЎўPH3µИЖшМеЈ¬РиК№УГ·в±ХЧ°ЦГЎЈРґіцУГCuSO4ИЬТєОьКХH2SЖшМеµД»ЇС§·ґУ¦·ЅіМКЅЈє____________________________
ўЪ·ґУ¦№эіМЦРК№УГ№эБїМъ·ЫµДДїµДКЗ____________________________
(3)ЦЖ±ё(NH4)2Fe(SO4)2Ў¤6H2OЈєПтFeSO4ИЬТєЦРјУИлТ»¶ЁЦКБїµД(NH4)2SO4№ММеЈ¬70~80ЎжМхјюПВИЬЅвєуЈ¬іГИИµ№Ил50mLТТґјЦРЈ¬Оціцѕ§МеЎЈ
КµСйЦРЈ¬Ри¶Ф№эВЛіцІъЖ·µДДёТє(pH<1)ЅшРРґ¦АнЎЈКТОВПВЈ¬·Ц±рИЎДёТєІўПтЖдЦРјУИлЦё¶ЁОпЦКЈ¬·ґУ¦єуµДИЬТєЦРЦчТЄґжФЪµДТ»ЧйАлЧУХэИ·µДКЗ_____ (МоРтєЕ)ЎЈ
A.НЁИл№эБїCl2ЈєFe2+ЎўH+ЎўNH4+ЎўClЎҐЎўSO42ЎҐ
B.јУИл№эБїKSCNИЬТєЈєK+ЎўNH4+ЎўFe3+ЎўSO42ЎҐЎўSCNЎҐ
C.јУИл№эБїNaOHИЬТєЈєNa+ЎўFe2+ЎўNH4+ЎўSO42ЎҐЎўOHЎҐ
D.јУИл№эБїNaClOєНNaOHµД»мєПИЬТєЈєNa+ЎўSO42ЎҐЎўClЎҐЎўClOЎҐЎўOHЎҐ
(4)ІъЖ·ґї¶ИІв¶ЁЈєіЖИЎagІъЖ·ИЬУЪЛ®Ј¬ЕдЦЖіЙ500mLИЬТєЈ¬ИЎ25.00mLґэІвТєЈ¬УГЕЁ¶ИОЄcmolЎ¤L-1µДЛбРФKMnO4ИЬТєµО¶ЁЎЈЦШёґЙПКцІЩЧч2ґОКµСйЅб№ыИзПВЈє

ёГІъЖ·µДґї¶ИОЄ____________________________(УГє¬aЎўcµДґъКэКЅ±нКѕ)ЎЈ
УРН¬С§МбіцЈ¬Ів¶ЁІъЖ·ЦРSO42ЎҐµДє¬БїТІїЙІв¶ЁІъЖ·µДґї¶ИЈ¬ЗлІ№ідНкХыКµСй·Ѕ°ёЈєіЖИЎФј0.4gСщЖ·Ј¬ИЬУЪ70mLЛ®Ј¬__________________________________________________Ј¬Ѕ«іБµнТЖИлЫбЫцЈ¬ЧЖЙХЦБєгЦШЈ¬јЗВјКэѕЭ(КµСйЦР±ШРлК№УГµДКФјБУРЈє2molЎ¤L-1µДHClИЬТєЎўBaCl2ИЬТєЎўAgNO3ИЬТє)ЎЈ
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com