
| m |
| M |
| 4.6g |
| 23g/mol |
| 2.4g |
| 24g/mol |
| 2.7g |
| 27g/mol |
| 6.4g |
| 64g/mol |
| 0.15mol |
| 2 |


科目:高中化学 来源: 题型:
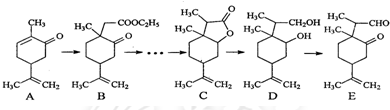
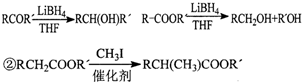
| HBr |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
| C、[H+]和[OH-]的乘积 | ||
| D、OH-的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠 | B、铜 | C、铝 | D、铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
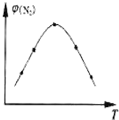 据报道,在一定条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,主要产物为NH3,相应的反应方程式为:2N2(g)+6H2O (g)?4NH3(g)+3O2(g)△H=Q kJ/mol
据报道,在一定条件下,N2在掺有少量氧化铁的二氧化钛催化剂表面能与水发生反应,主要产物为NH3,相应的反应方程式为:2N2(g)+6H2O (g)?4NH3(g)+3O2(g)△H=Q kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:
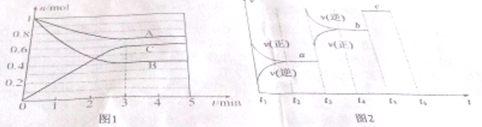
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1s22s22p63s23p2→1s22s22p63s23p1 |
| B、1s22s22p2→1s22s22p1 |
| C、1s22s22p4→1s22s22p3 |
| D、1s22s22p3→1s22s22p2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从海水中可以得到NaCl |
| B、海水蒸发制海盐的过程中只发生了化学变化 |
| C、海水中含有碘元素,将海水中的碘升华就可以得到碘单质 |
| D、利用潮汐发电是将化学能转化为电能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com