
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同, b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题:
(1)b、c、d中第一电离能最大的是 (填元素符号),e的价层电子轨道示意图为 。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为 ;分子中 既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写两种)。
既含有极性共价键,又含有非极性共价键的化合物是 (填化学式,写两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是 ;酸根呈三角锥结构的酸是 。(填化学式)
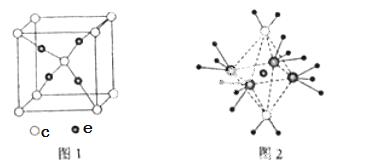
(4)e和c形成的一种离子化合物的晶体结构如图1,则e离子的电荷为 。
(5)这5种元素形成 的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中阴离子为 ,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是
的一种1:1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构(如图2所示)。该化合物中阴离子为 ,阳离子中存在的化学键类型有 ;该化合物加热时首先失去的组分是  ,判断理由是 。
,判断理由是 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列化学用语正确的是:( )
A.Cl-的结构示意图: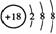
B.光导纤维主要成分的化学式:Si
C.1H2、2H2、3H2互为同位素
D.质子数为53,中子数为78的碘原子:131 53I
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)火法炼锌是将闪锌矿(主要成分是ZnS)通过浮选焙烧使它转化为氧化锌,再把氧化锌和焦炭混合,在鼓风炉中加热到1 100~1 300 ℃,使锌蒸馏出来。
①写出火法炼锌的主要反应:
焙烧反应:_________________________________________。
鼓风炉中可能发生的反应:___________________(任写一个)
②从保护环境和充分利用原料角度看如何处理和利用产生的烟气?_____________________________________________________________________________。
(2)工业上冶炼铝就是电解氧化铝
①冶炼铝的电解槽中的阴极和阳极材料均用石油炼制和煤的干馏产品________(填物质名称)。
②氧化铝的熔点很高,在铝的冶炼中要加入冰晶石(Na3AlF6),其作用是________________________________________________。
③工业上冶炼铝时用的原料是Al2O3,而不是AlCl3,其原因是
______________________________________________________。
(3)工业上“联合制碱法”中主要反应的化学方程式是_______________________________________。
其中的CO2来源于______________。
(4)碳酸钙是制玻璃的原料之一,工业上制玻璃是在玻璃熔炉中进行,其中反应之一为CaCO3+SiO2 CaSiO3+CO2↑,若在上述条件下,把1 000a g CaCO3和60a g SiO2混合,则生成的CO2在标准状况下的体积为________________(用含a的代数式表示)。
CaSiO3+CO2↑,若在上述条件下,把1 000a g CaCO3和60a g SiO2混合,则生成的CO2在标准状况下的体积为________________(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
电石浆是氯碱工业中的一种废弃物,其大致组成如下表所示:
| 成分 | CaO | SiO2 | Al2O3 | Fe2O3 | MgO | CaS | 其他不溶于酸的物质 |
| 质量分数 (%) | 65~66 | 3.5~5.0 | 1.5~3.5 | 0.2~0.8 | 0.2~1.1 | 1.0~1.8 | 23~26 |
用电石浆可生产无水CaCl2,某化工厂设计了以下工艺流程:
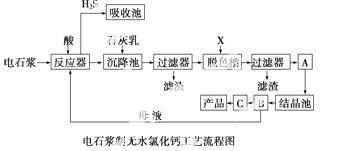
已知氯化钙晶体的化学式是CaCl2·6H2O;H2S是一种酸性气体,且具有还原性。
(1)反应器中加入的酸应选用 ________。
(2)脱色槽中应加入的物质X是______________;设备A的作用是______________;设备B的名称为 ______________;设备C的作用是 ____________。
(3)为了满足环保要求,需将废气H2S通入吸收池,下列物质中最适合作为吸收剂的是________。
A.水 B.浓硫酸 C.石灰乳 D.硝酸
(4)将设备B中产生的母液重新引入反应器的目的是__________________________
______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氯化铝的熔点为190 ℃(2.02×106 Pa),但它在180 ℃即开始升华。
(1)氯化铝是________(填“离子晶体”或“分子晶体”)。
(2)在500 K和1.01×105 Pa时,它的蒸气密度(换算成标准状况时)为11.92 g·L-1,试确定氯化铝在蒸气状态的化学式为________,微粒间的作用力类型有________。
(3)无水氯化铝在空气中强烈地“发烟”,其原因是______________________。
(4)设计一个更可靠的实验,判断氯化铝是离子晶体还是分子晶体,你设计的实验是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一水硫酸四氨合铜(Ⅱ)([Cu(NH3)4]SO4·H2O)是一种重要的染料及农药中间体。请回答下列相关问题:
(1)Cu的核外电子排布式为 。
(2)N的L层中有 对成对电子;N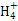 立体构型是 ,其中心原子的杂化方式为 。
立体构型是 ,其中心原子的杂化方式为 。
(3)氨水溶液中存在多种氢键,任表示出其中两种 ;
(4)[Cu(NH3)4]SO4·H2O中呈深蓝色的离子是 ,该微粒中的“电子对给予一接受键”属于 键;
(5)Cu的一种氯化物晶胞结构如图所示,该氯化物的化学式 。
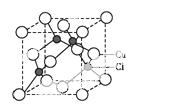
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、M、D、E是原子序数依次增大的五种短周期元素。A元素的一种原子中不含中子。B、M、D、E分别在下表(周期表的一部分)不同的空格内占有相应的位置,E的原子序数是D的原子序数的2倍。试回答:
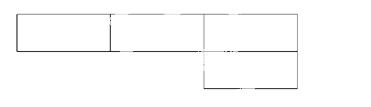
(1)将D、E的元素符号分别填在相应的空格内。
(2)在B、M、D、E四种元素的最简单氢化物中,沸点最高的是__________(填化学式)B、M的最简单氢化物的空间构型分别为________、____ ____。
____。
(3)A、B、M、D可组成多种18电子分子,其中两种的结构可分别表示为A2M—MA2和BA3—MA2,请根据这两种分子的结构特点再写出2种具有18电子的有机物的结构简式__________、__________(用元素符号表示)。
(4)D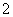 存在于人体中,能使人过早衰老,但在催化剂存在下很快转化为A2D2、D2等物质,该转化过程可用离子方程式表示为______+______H2O
存在于人体中,能使人过早衰老,但在催化剂存在下很快转化为A2D2、D2等物质,该转化过程可用离子方程式表示为______+______H2O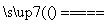 ______+________+______,其中A2D2中所含化学键类型有________。
______+________+______,其中A2D2中所含化学键类型有________。
(5)由C原子构成C60,其晶体类型为________,由M最高价氧化物与其气态氢化物反应生成的物质为________,其晶体类型为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
无色有刺激性气味的SO2气体与含1.5 mol Cl的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5NA个电子转移时,该反应的化学方程式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.12.5mL 16mol·L-1浓硫酸与足量锌反应,转移电子数为0.2NA
B.0.1 mol24Mg18O晶体中所含中子总数为2.0 NA
C.1L 1 mol·L-1的醋酸溶液中离子总数为2NA
D.4.5 g SiO2晶体中含有的硅氧键数目为0.3 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com