
【题目】部分氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共2.88g,经如下处理:

下列说法正确的是
A.滤液A中的阳离子为Fe2+、Fe3+、H+B.V=224
C.样品中CuO的质量为2.0gD.样品中铁元素的质量为0.56g
【答案】B
【解析】
根据氧化性Fe3+>Cu2+>H+可知铁离子优先反应,由于滤液A中不含Cu2+,且有气体氢气生成,则滤液A中不含Fe3+,滤渣1.6g为金属铜,物质的量为0.025mol,即合金样品中总共含有铜原子和铜离子0.025mol。滤液A中加入足量氢氧化钠溶液,所得滤渣灼烧得到的固体为Fe2O3,质量为1.6g,物质的量为0.01mol,即合金样品中总共含有铁原子和铁离子0.02mol。稀硫酸过量,因此滤液A中的溶质为H2SO4和FeSO4,其中溶质FeSO4为0.02mol,则能加反应的硫酸的物质的量也为0.02mol,0.02mol H2SO4电离出0.04mol氢离子,其中部分氢离子生成氢气,另外的H+和合金中的氧离子O2-结合成水。
A、滤液A中的阳离子为Fe2+、H+,选项A错误;
B、合金中氧离子O2-的物质的量为![]() =0.01mol,0.01mol O2-生成水需结合H+0.02mol,所以参加反应的0.02mol硫酸中有0.04mol-0.02mol=0.02molH+生成了氢气,即有0.01molH2生成,标准状况下产生的氢气的体积为0.01mol
=0.01mol,0.01mol O2-生成水需结合H+0.02mol,所以参加反应的0.02mol硫酸中有0.04mol-0.02mol=0.02molH+生成了氢气,即有0.01molH2生成,标准状况下产生的氢气的体积为0.01mol![]() 22.4L/mol=0.224L=224mL,选项B正确;
22.4L/mol=0.224L=224mL,选项B正确;
C、假设Fe-Cu合金样品全部被氧化,则样品中CuO的质量为0.025mol![]() 80g/mol=2g,而实际情况是Fe-Cu合金样品部分氧化,故样品中CuO的质量小于2g,选项C错误;
80g/mol=2g,而实际情况是Fe-Cu合金样品部分氧化,故样品中CuO的质量小于2g,选项C错误;
D、样品中铁元素的质量为0.02mol![]() 56g/mol=1.12g,选项D错误。
56g/mol=1.12g,选项D错误。
答案选B。


科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,不合理的是( )
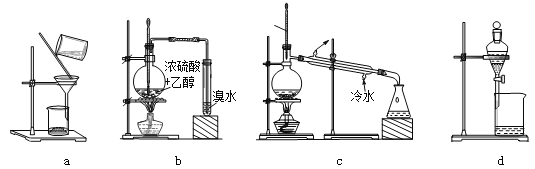
A. 用a趁热过滤提纯苯甲酸B. 用b制备并检验乙烯
C. 用c除去溴苯中的苯D. 用d分离硝基苯与水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数,下列叙述中正确的是:
A.标准状况下,2.24 L CHCl3中含有Cl原子的个数为0.3NA
B.1molCH4分子中共用电子个数为10NA
C.1molC2H6O分子中含有的C-H键的数目一定为5NA
D.14g乙烯和丙烯的混合物,完全燃烧后所生成的CO2分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘主要富集在海带中,我国海带产量居世界第一位,除供食用外,大量用于制碘。提取碘的途径如下图所示,下列有关叙述正确的是
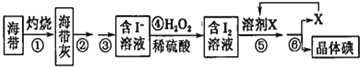
A.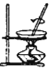 此装置进行操作①
此装置进行操作①
B.②③操作中所用到的玻璃仪器有:玻璃棒、烧杯、分液漏斗
C.④中当1molH2O2氧化I-时,转移电子数为2NA
D.溶剂X可选用酒精或苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数,下列说法不正确的是( )
A.1.5 mol NO2与足量的H2O反应,转移的电子数为NA
B.常温常压下,18g D2O含有的原子数为3NA
C.氧气和臭氧的混合物32 g中含有2NA个氧原子
D.在标准状况下,0.5NA个氯气分子所占体积约是11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机化合物可根据其组成和性质进行分类。
(1)如图所示的物质分类方法的名称是______________。
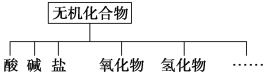
(2)
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①HCl ②______ | ③________ ④Ba(OH)2 | ⑤Na2CO3 ⑥_______ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在上表中②③⑥后面。
(3)写出⑦转化为⑤的化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2.4gRSO4中含0.02molR2+,则RSO4的摩尔质量是____;R的相对原子质量约是___。
(2)除去下列物质中所混有的少量杂质,指明应加入的试剂,写出有关的离子方程式。
NaHCO3溶液(Na2CO3):试剂_________,离子方程式:___________。
(3)实验室需要0.1mol/L的硫酸980mL,欲用密度为1.84g/cm3、溶质的质量分数为98%的浓硫酸进行配制,则需用量筒量取______mL进行配制。假如其他操作均准确无误,若使用量筒量取时俯视读数,最终所配溶液的浓度________(选填“偏高”、“偏低”或“无影响”);若溶解时未冷却,直接转移到容量瓶中至刻度线,最终所配溶液的浓度_________(选填“偏高”、“偏低”或“无影响”)。
(4)实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是__。反应化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式表达正确的是( )
A.向硫酸铁溶液中加入过量铁粉:Fe+2Fe3+=3Fe2+
B.向Na2CO3溶液中滴加稀盐酸:Na2CO3+2H+=2Na++CO2↑+H2O
C.向铜粉中加入稀硫酸:Cu+2H+=Cu2++H2↑
D.向铝粉中加入足量NaOH溶液:2Al+2OH-=2AlO![]() +H2↑
+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L恒容密闭容器中投入一定量的A、B发生反应:3A(g)+bB(g)![]() cC(g) H=-QkJ·mol-1(Q>0),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是
cC(g) H=-QkJ·mol-1(Q>0),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是
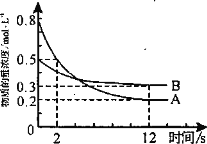
A. 2s时,A的反应速率为0.15mol·L-1·s-1
B. 图中交点时A的消耗速率等于A的生成速率
C. 化学计量数之比b ∶c = 1∶2
D. 12s内反应放出0.2QkJ热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com